题目内容
(2003?潍坊)一定质量的氯化铜和40g盐酸组成的混合溶液中慢慢滴入20%的氢氧化钠溶液并振荡,所加氢氧化钠溶液的质量与生成沉淀的质量的关系如图所示,下列判断中正确的是( )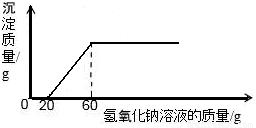
【答案】分析:在有酸存在的情况下,碱总是先与酸反应,等把酸完全消耗掉之后才与其它物质发生反应,所以本题中所发生反应的先后顺序为:(1)NaOH+HCl═NaCl+H2O,(2)CuCl2+2NaOH═Cu(OH)2↓+2NaCl 从图中可以分析出第一个反应所消耗的氢氧化钠溶液的质量为20g,第二个反应所消耗的氢氧化钠溶液的质量为40g.
解答:解:A、设生成沉淀的质量为x,则:
CuCl2+2NaOH═Cu(OH)2↓+2NaCl
80 98
40g x20%=8g x
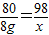
解得:x=9.8g
故A错.
B、设盐酸的质量分数为y,则:
NaOH+HCl═NaCl+H2O
40 36.5
20gx20% 40g?y
=4g
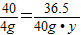
解得:y=9.125%
故B错.
C选项说的不严密,一开始加入氢氧化钠溶液不会产生沉淀,到最后把氯化铜消耗完之后,也不会再产生沉淀故 C错
D由上分析中所发生的两个化学反应及图可知,加入60g氢氧化钠溶液时,恰好把氯化铜和盐酸消耗掉,所以最后所得溶液中的溶质只有氯化钠也就是氯化钠溶液,故D正确.
故选D
点评:这类题应该首先分析所发生的化学反应,然后根据反应的化学方程式及题给条件进行求算,如果学生熟练掌握酸碱盐两两之间的反应,及根据化学方程式的计算,这些问题都很容易解决了.
解答:解:A、设生成沉淀的质量为x,则:
CuCl2+2NaOH═Cu(OH)2↓+2NaCl
80 98
40g x20%=8g x
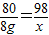
解得:x=9.8g
故A错.
B、设盐酸的质量分数为y,则:
NaOH+HCl═NaCl+H2O
40 36.5
20gx20% 40g?y
=4g
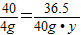
解得:y=9.125%
故B错.
C选项说的不严密,一开始加入氢氧化钠溶液不会产生沉淀,到最后把氯化铜消耗完之后,也不会再产生沉淀故 C错
D由上分析中所发生的两个化学反应及图可知,加入60g氢氧化钠溶液时,恰好把氯化铜和盐酸消耗掉,所以最后所得溶液中的溶质只有氯化钠也就是氯化钠溶液,故D正确.
故选D
点评:这类题应该首先分析所发生的化学反应,然后根据反应的化学方程式及题给条件进行求算,如果学生熟练掌握酸碱盐两两之间的反应,及根据化学方程式的计算,这些问题都很容易解决了.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(2003?潍坊)依据化学实验事实分析、归纳结论,并根据结论推测同类物质的性质,是一种科学的学习方法.请你仿照表中的示例,以所学过的酸、碱、盐的化学性质为例,填写表中的所有空格.(所填实验结论不能重复)
| 实验事实 (至少举两例) | 实验结论 | 结论应用 (举例说明) |
| 例:氢氧化钠、氢氧化铜都能跟盐酸反应,生成盐和水 | 碱能跟盐酸反应,生成盐和水 | 氢氧化钾溶液也能跟盐酸反应,生成盐和水 |
| (1)盐酸、稀硫酸都能使紫色石蕊试液变红 | 酸溶液能使紫色石蕊试液变红 | ______ |
| (2)氯化钠、氯化钾溶液都能与硝酸银溶液反应,生成不溶于稀硝酸的白色沉淀 | ______ | ______ |
| (3)______ | ______ | ______ |