题目内容
16.如图甲是A、B、C三种固体物质的溶解度曲线图: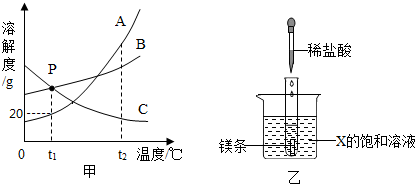
(1)甲图中,P点所表示的含义为在t1℃时,B、C的溶解度相等.
(2)将B 物质的不饱和溶液转变饱和溶液可采取的方法有加溶质(写1种方法).
(3)在t1℃时,将30gA物质完全溶解于蒸馏水中可得到A的饱和溶液180g.
(4)t2℃时,将等质量的三种物质的饱和溶液分别降至t1时,析出晶体最多的是A.
(5)如图乙所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的C.若要生成氢气0.1g,则至少需要镁条的质量为1.2g.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,甲图中,P点所表示的含义为:在t1℃时,B、C的溶解度相等;
(2)B物质的溶解度随温度的升高而增大,所以将B物质的不饱和溶液转变饱和溶液可采取的方法有加溶质或蒸发溶剂;
(3)在t1℃时,A物质的溶解度是20g,所以将30gA物质完全溶解于蒸馏水中可得到A的饱和溶液180g;
(4)t2℃时,甲物质的溶解度最大,t1℃时,甲物质的溶解度最小,所以将等质量的三种物质的饱和溶液分别降至t1时,析出晶体最多的是A;
(5)镁和盐酸反应放出热量,所以20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的C,依据化学方程式:Mg+2HCl=MgCl2+H2↑可知,24份质量的镁会生成2份质量的氢气,所以要生成氢气0.1g,则至少需要镁条的质量为1.2g.
故答案为:(1)在t1℃时,B、C的溶解度相等;
(2)加溶质;
(3)180;
(4)A;
(5)1.2.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
6.生活、生产中处处离不开化学知识,下列说法中错误的是( )
| A. | 用甲醛浸泡蔬菜的根部,可以延长其保鲜期 | |
| B. | 地沟油经化学方法处理后制成航空燃油,可实现变废为宝 | |
| C. | 闻到家中煤气泄漏时,不能按动排气扇等电器的开关 | |
| D. | 在火场浓烟中逃生,可用湿毛巾捂住口鼻,蹲下靠近地面或沿墙壁跑离着火区域 |
11.复方篙甲醚(C16H26O5)是一种治疗疟疾的有效药品,下列说法正确的是( )
| A. | 复方篙甲醚属于有机物 | |
| B. | 复方篙甲醚由47个原子构成 | |
| C. | 复方篙甲醚中C、H、O三种元素质量比是16:26:5 | |
| D. | 复方篙甲醚中碳元素的质量分数是$\frac{12}{12×16+1×26+16×5}$×100% |
8.某化学反应可以用X+Y→M+R表示,下列关于此反应的说法中,正确的是( )
| A. | 若X是单质,则该反应一定是置换反应 | |
| B. | 若Y为金属,则该反应一定生成氢气 | |
| C. | 若X为紫红色金属,则该反应在常温下进行时一定生成蓝色溶液 | |
| D. | 若参加反应的X和Y的质量之和为10g,则生成M和R的质量之和一定是10g |
1.把一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如表.下列说法不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量(g) | 4.0 | 2.0 | 3.0 | 2.0 |
| 反应后的质量(g) | 1.2 | X | 2.4 | 5.4 |
| A. | 参加反应的甲、丙质量比是1:2 | B. | 丁一定是化合物 | ||
| C. | X=2.0,乙可能是催化剂 | D. | 此反应基本类型为化合反应 |