题目内容
10.熟悉化学方程式是领悟化学反应实质的重要途径,请用化学方程式填写在相关空白处.(1)生锈的铁钉放入过量的稀盐酸中溶液变成黄色(用化学方程式表示)Fe2O3+6HCl═2FeCl3+3H2O;片刻后,有气泡产生的原因(用化学方程式表示)Fe+2HCl═FeCl2+H2↑.
(2)已知NH4Cl与Ca(OH)2混合研磨要产生NH3、H2O和一种盐.请写出该反应的化学方程式Ca(OH)2+2NH4Cl═CaCl2+2H2O+2NH3↑.
(3)农业经常用熟石灰与硫酸铜配置波尔多液来作杀虫剂,但是在配置好的波尔多液不能用铁制容器盛放(用化学方程式表示)Fe+CuSO4=FeSO4+Cu.
(4)上述共计四个反应中,其中有2个反应属于复分解反应类型.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
复分解反应是两种化合物相互交换成分生成两种新的化合物的反应.
解答 解:(1)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;片刻后,有气泡产生,是因为铁与稀盐酸反应生成氯化亚铁溶液和氢气,反应的化学方程式是:Fe+2HCl═FeCl2+H2↑.
(2)NH4Cl与Ca(OH)2混合研磨要产生NH3、H2O和一种盐(由质量守恒定律,反应前后元素种类不变,该盐是氯化钙),反应的化学方程式为:Ca(OH)2+2NH4Cl═CaCl2+2H2O+2NH3↑.
(3)铁的活动性比铜强,铁和硫酸铜反应会生成硫酸亚铁溶液和铜,不能用铁制容器配制波尔多液,反应的化学方程式为:Fe+CuSO4=FeSO4+Cu.
(4)上述共计四个反应中,Fe2O3+6HCl═2FeCl3+3H2O、Ca(OH)2+2NH4Cl═CaCl2+2H2O+2NH3↑(氨气和水可看作是氨水分解得到的)是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应.
故答案为:(1)Fe2O3+6HCl═2FeCl3+3H2O;Fe+2HCl═FeCl2+H2↑;(2)Ca(OH)2+2NH4Cl═CaCl2+2H2O+2NH3↑;(3)Fe+CuSO4=FeSO4+Cu;(4)2.
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法(写、配、注、等)、复分解反应的特征即可正确解答本题.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
1.氨气是一种有强烈刺激性气味的气体,密度比空气小,极易溶于水,应该用何种方法收集该气体( )
| A. | 向上排空气法 | B. | 向下排空气法 | C. | 排水法 | D. | 排空气法 |
18.现代客机外壳主要材料是铝锂合金.锂的原子结构示意图为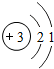 ,下列关于锂的说法错误的是( )
,下列关于锂的说法错误的是( )
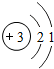 ,下列关于锂的说法错误的是( )
,下列关于锂的说法错误的是( )| A. | 锂元素属于金属元素 | B. | 锂原子的质子数为3 | ||
| C. | 锂元素在化合物中通常显+2价 | D. | 锂原子在化学反应中容易失去电子 |
5.下列实验中可观察到明显现象的是( )
| A. | 向盐酸中滴加氢氧化钠溶液 | B. | 向氯化铜溶液中滴加硝酸钾 | ||
| C. | 向氯化镁溶液中滴加氢氧化钡溶液 | D. | 将铜丝放入到硫酸铝溶液中 |
15.某K2CO3样品,一定含Na2CO3、NaCl和BaCl2杂质中的一种或两种,将13.8g样品加入足量水,样品全部溶解形成无色溶液,往溶液中加入过量的CaCl2溶液,得到9g沉淀,对样品所含杂质的判断正确的是( )
| A. | 肯定有NaCl | B. | 一定没有BaCl2,可能有NaCl | ||
| C. | 肯定有NaCl,还可能有Na2CO3 | D. | 肯定没有Na2CO3和BaCl2 |
2.下列化肥属于复合肥的是( )
| A. | NH4H2PO4 | B. | Ca(H2PO4)2+CaSO4 | C. | K2SO4 | D. | NH4HCO3 |
19.下列有关生活的化学知识,正确的是( )
| A. | 酸雨是指PH小于7的雨水 | B. | 可用氢氧化钠改良酸性土壤 | ||
| C. | 甲醛溶液用于食品保鲜 | D. | 灼烧闻气味区分蚕丝和棉纱 |
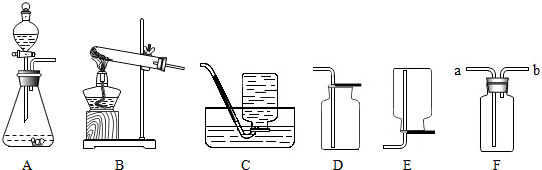
 (1)用化学符号表示:
(1)用化学符号表示: