题目内容
10.除去下列物质中的杂质(括号内为杂质)、写出所加试剂(1)Ag(Cu)硝酸银溶液 (2)Cu(CuO)稀盐酸 (3)CuO(Cu)在氧气中加热
(4)C(CuO)稀盐酸 (5)Cu(Fe)稀盐酸 (6)CO(CO2)氢氧化钠溶液
(7)BaSO4(MgO)稀盐酸 (8)KNO3(KCl)硝酸银溶液 (9)HNO3(H2SO4)硝酸钡溶液
(10)FeSO4(CuSO4)铁粉 (11)Na2SO4(Na2CO3)稀硫酸 (12)NaCl(NaOH)稀盐酸.
分析 本题属于除杂质题,一般的除杂质题必须同时满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应②反应时不能加入新的杂质.银中的杂质铜可以用硝酸银溶液除去;Cu中的杂质CuO,可以用稀盐酸除去,然后过滤即可;CuO中的杂质Cu可以在氧气中加热,铜和氧气生成氧化铜;C中的杂质CuO可以用稀盐酸或稀硫酸除去,然后过滤;Cu中杂质Fe可以用稀盐酸除去,或稀硫酸除去,然后过滤;CO中的杂质CO2可以用氢氧化钠溶液除去;BaSO4中的杂质MgO可以用稀盐酸或稀硫酸除去,然后过滤;KNO3中的杂质KCl,可以用硝酸银溶液除去,然后过滤;HNO3中的杂质H2SO4可以用硝酸钡溶液除去,生成硫酸钡和硝酸,过滤即可;FeSO4中的杂质CuSO4可以用铁粉除去,然后过滤即可;Na2SO4中的杂质Na2CO3可以用稀硫酸除去,生成硫酸钠和水和二氧化碳;NaCl中的杂质NaOH可以用稀盐酸除去,生成氯化钠和水.
解答 解:一般的除杂质题必须同时满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应②反应时不能加入新的杂质.银中的杂质铜可以用硝酸银溶液除去;Cu中的杂质CuO,可以用稀盐酸除去,然后过滤即可;CuO中的杂质Cu可以在氧气中加热,铜和氧气生成氧化铜;C中的杂质CuO可以用稀盐酸或稀硫酸除去,然后过滤;Cu中杂质Fe可以用稀盐酸除去,或稀硫酸除去,然后过滤;CO中的杂质CO2可以用氢氧化钠溶液除去;BaSO4中的杂质MgO可以用稀盐酸或稀硫酸除去,然后过滤;KNO3中的杂质KCl,可以用硝酸银溶液除去,然后过滤;HNO3中的杂质H2SO4可以用硝酸钡溶液除去,生成硫酸钡和硝酸,过滤即可;FeSO4中的杂质CuSO4可以用铁粉除去,然后过滤即可;Na2SO4中的杂质Na2CO3可以用稀硫酸除去,生成硫酸钠和水和二氧化碳;NaCl中的杂质NaOH可以用稀盐酸除去,生成氯化钠和水;故答案为:(1)硝酸银溶液;(2)稀盐酸;(3)在氧气中加热;(4)稀盐酸;(5)稀盐酸;(6)氢氧化钠溶液;(7)稀盐酸;(8)硝酸银溶液;(9)硝酸钡溶液;(10)铁粉;(11)稀硫酸;(12)稀盐酸;
点评 本考点属于物质的除杂或净化的探究,是中考的一个难点,也是学生经常出错的题型.根据物质的溶解性和除杂质的条件,要认真分析,综合把握.还要加强记忆除去常用离子的方法和物质的溶解性,从而突破难点,本考点经常出现在选择题、填空题和实验题中.

 应用题作业本系列答案
应用题作业本系列答案| A. | 相对原子质量为58 | B. | 中子数为58 | ||
| C. | 相对原子质量为140.1g | D. | 质子数为58 |
①用pH试纸测试溶液的pH; ②用光学显微镜观察; ③用嘴尝;
④滴加FeCl3溶液; ⑤通入二氧化碳;⑥加入碳酸钠溶液.
其中可行的是( )
| A. | ①②④ | B. | ③④⑤⑥ | C. | ①④⑤ | D. | ⑤⑥ |
| A. | 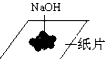 称量固体 | B. | 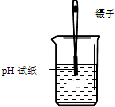 测定溶液pH | C. | 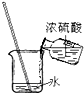 稀释浓硫酸 | D. |  滴加液体 |
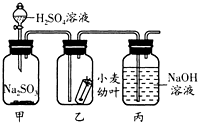 针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠(Na2SO3)反应可产生硫酸钠和二氧化硫和水.设计实验如图所示.
针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠(Na2SO3)反应可产生硫酸钠和二氧化硫和水.设计实验如图所示.(1)写出产生二氧化硫的化学方程式Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;
(2)在实验中,丙装置的作用是吸收未反应的二氧化硫,防止污染空气;
(3)其他实验条件相同情况下,该小组观察到小麦幼叶在不同光照强度下,叶片发生变化时间不同,如下表所示.结合叶的结构知识,请你解释为何光照的强弱会影响二氧化硫对植物的危害?光照的强弱会影响叶表皮气孔的开放程度,进而导致二氧化硫对植物的危害随光照的加强而增大.
| 室内 | 阳光下 | ||
| 出现烟斑时间 | 叶片变黄时间 | 出现烟斑时间 | 叶片变黄时间 |
| 30分钟 | 38分钟 | 15分钟 | 23分钟 |
| A. | 若生成物C、D中有一种为单质,则该反应一定是置换反应 | |
| B. | 若生成物C和D分别为两种沉淀,A、B有可能为盐和碱 | |
| C. | 若C、D是盐和水,则A、B一定是酸和碱 | |
| D. | 若A、B、C、D都是化合物,则该反应一定是复分解反应 |