题目内容
同温、同压下,相同体积的气体具有相同的分子数.今有氢气和一氧化碳的混合气体VL,当其完全燃烧时,需要同温同压下的氧气0.5VL,则混合气体中H2和CO的体积比是( )
| A、1:1 | B、1:2 | C、1:3 | D、不能确定 |
分析:由于氢气与一氧化碳相互间不发生反应,它们都与氧气反应分别生成水和二氧化碳,根据两者与氧气反应的化学方程式,可判断反应时的分子个数比,即气体的体积比,通过对比可发现相同体积的氢气与一氧化碳反应消耗氧气的体积相同,因此,可对混合气体中H2和CO的体积比做出为任意比的判断.
解答:解:根据反应的化学方程式,2CO+O2
2CO2、2H2+O2
2H2O,每2个CO分子反应消耗1个氧气分子、每2个H2分子反应也消耗1个氧气分子,由同温、同压下,相同体积的气体具有相同的分子数,可知相同体积的氢气与一氧化碳反应消耗氧气的体积相同,即每体积CO或H2完全反应都需要消耗0.5体积的氧气,因此混合气体中H2和CO的体积比为任意比.
故选D.
| ||
| ||
故选D.
点评:由题目所给“同温、同压下,相同体积的气体具有相同的分子数”信息,得到分子数比即体积比,体现出获得信息、处理信息的能力.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
 (石油液化气的主要成分)混合,所得混合气体中,碳、氢、氧元素的质量比为________.
(石油液化气的主要成分)混合,所得混合气体中,碳、氢、氧元素的质量比为________.
 ,
, .煤气灶是由灶体、进气管、进风管、电子开关等部件组成.目前管道煤气的用户迅速增加.根据以上反应分析,一个使用石油液化气的用户,在使用管道煤气后,重新购置的灶具与原来的灶具相比结构上的最大区别是________;原因是________________________.
.煤气灶是由灶体、进气管、进风管、电子开关等部件组成.目前管道煤气的用户迅速增加.根据以上反应分析,一个使用石油液化气的用户,在使用管道煤气后,重新购置的灶具与原来的灶具相比结构上的最大区别是________;原因是________________________.
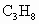 (石油液化气的主要成分)混合,所得混合气体中,C、H、O元素的质量比是________.
(石油液化气的主要成分)混合,所得混合气体中,C、H、O元素的质量比是________.
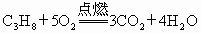 ,
,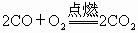 .燃气灶是由灶体、进气管、进风管、电子开关等部件组成.目前管道煤气的用户迅速增加.根据以上反应分析,使用石油液化气的用户,在使用管道煤气后,重新购置的灶具与原来的灶具相比构造上的最大区别是________;原因是________.
.燃气灶是由灶体、进气管、进风管、电子开关等部件组成.目前管道煤气的用户迅速增加.根据以上反应分析,使用石油液化气的用户,在使用管道煤气后,重新购置的灶具与原来的灶具相比构造上的最大区别是________;原因是________.
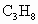 (石油液化气的主要成分)混合,所得混合气体中,碳、氢、氧元素的质量比为________.
(石油液化气的主要成分)混合,所得混合气体中,碳、氢、氧元素的质量比为________.
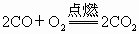 ,
, .煤气灶是由灶体、进气管、进风管、电子开关等部件组成.目前管道煤气的用户迅速增加.根据以上反应分析,一个使用石油液化气的用户,在使用管道煤气后,重新购置的灶具与原来的灶具相比结构上的最大区别是________;原因是________________________.
.煤气灶是由灶体、进气管、进风管、电子开关等部件组成.目前管道煤气的用户迅速增加.根据以上反应分析,一个使用石油液化气的用户,在使用管道煤气后,重新购置的灶具与原来的灶具相比结构上的最大区别是________;原因是________________________.
 (石油液化气的主要成分)混合,所得混合气体中,C、H、O元素的质量比是________.
(石油液化气的主要成分)混合,所得混合气体中,C、H、O元素的质量比是________.
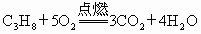 ,
, .燃气灶是由灶体、进气管、进风管、电子开关等部件组成.目前管道煤气的用户迅速增加.根据以上反应分析,使用石油液化气的用户,在使用管道煤气后,重新购置的灶具与原来的灶具相比构造上的最大区别是________;原因是________.
.燃气灶是由灶体、进气管、进风管、电子开关等部件组成.目前管道煤气的用户迅速增加.根据以上反应分析,使用石油液化气的用户,在使用管道煤气后,重新购置的灶具与原来的灶具相比构造上的最大区别是________;原因是________.