题目内容
15.在100g双氧水中加入5g二氧化锰,完全反应后,称的剩余物的总质量为101.8g,则生成氧气的质量为多少克?双氧水中过氧化氢的质量为多少克?剩余物中有什么物质?各多少克?分析 双氧水在二氧化锰的催化作用下生成水和氧气,由质量守恒定律,混合物减少的质量即为生成氧气的质量,由生成氧气的质量、由反应的化学方程式列式计算出双氧水中过氧化氢的质量即可.
解答 解:由质量守恒定律,生成氧气的质量为100g+5g-101.8g=3.2g.
设常见反应的过氧化氢的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 3.2g
$\frac{68}{32}=\frac{x}{3.2g}$ x=6.8g.
剩余物质中含有水、二氧化锰,二氧化锰作催化剂,反应前后质量不变,二氧化锰的质量为5g;则剩余物中水的质量为101.8g-5g=96.8g.
答:生成氧气的质量为3.2g;双氧水中过氧化氢的质量为6.8g;水、二氧化锰;96.8g;5g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氧气的质量是正确解答本题的前提和关键.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
5.如图所示的四个图象,能正确反映对应变化关系的是( )
| A. | 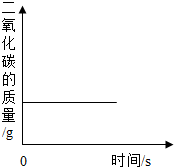 一定质量的木炭在密闭的容器内燃烧 | |
| B. | 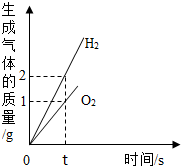 水的电解 | |
| C. | 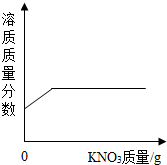 20℃时,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体 | |
| D. | 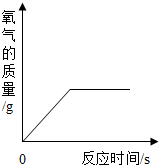 利用一定量的过氧化氢溶液制氧气 |
10.用你最熟悉的三种元素完成下列表格
| 元素名称 | 元素符号 | 常见化合价 | 组成化合物的化学式(两种即可,但一种化学式不能在表格中重复出现) |
| 1 |
7.下列叙述正确的是( )
| A. | 2g H2与1g O2充分反应后生成3g水 | |
| B. | 1g H2与1g O2充分反应后生成2g水 | |
| C. | 2g H2与16g O2充分反应后生成18g水 | |
| D. | 16g H2与2g O2充分反应后生成18g水 |
 水是一切生物体的最基本组成成分,如图为测定水的组成实验装置,计算:
水是一切生物体的最基本组成成分,如图为测定水的组成实验装置,计算: