题目内容
15.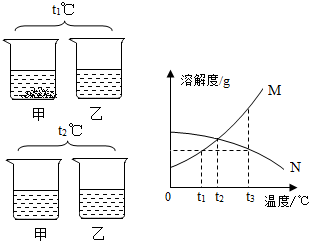 甲、乙两种物质的溶解度曲线如图.t1℃时,在两烧杯中分别加入等质量的两种物质和等质量的蒸馏水,充分溶解后现象如图;继续加热到t2℃时现象如图(不考虑溶剂质量变化).下列说法不正确的是( )
甲、乙两种物质的溶解度曲线如图.t1℃时,在两烧杯中分别加入等质量的两种物质和等质量的蒸馏水,充分溶解后现象如图;继续加热到t2℃时现象如图(不考虑溶剂质量变化).下列说法不正确的是( )| A. | t1℃时甲一定是饱和溶液 | |
| B. | t2℃时甲、乙两溶液的溶质质量分数相等 | |
| C. | t2℃时甲、乙两溶液一定均为不饱和溶液 | |
| D. | 图中M表示甲的溶解度曲线 |
分析 A、根据t1℃时图示分析;
B、根据溶质质量分数的计算公式分析;
C、根据饱和溶液及不饱和溶液的概念和溶解度曲线分析;
D、根据温度变化时溶解度的变化情况分析.
解答 解:A、t1℃时,甲物质仍有部分不溶性固体,所以一定是饱和溶液,故正确;
B、t2℃时甲、乙两溶液加入等质量的两种物质和等质量的蒸馏水,并且都完全溶解,所以甲、乙两溶液的溶质质量分数相等,故正确;
C、由于甲物质升高温度是会继续溶解,所以甲物质的溶解度曲线为M,t2℃时,无法判断是否饱和;则乙物质的溶解度曲线为N,其溶解度会随着温度的升高而减小,所以t2℃时,乙物质也可能为饱和溶液,故错误;
D、t1℃时,甲物质仍有部分不溶性固体,继续加热到t2℃时,全部溶解,说明甲物质的溶解度随温度的升高而增大,所以甲物质的溶解度曲线为M,故正确.
故选:C.
点评 本题既考查了溶解度曲线的应用,又考查了对于饱和溶液的理解,溶质的质量分数判断,是一道较好的培养学生分析、解决问题能力的题目.

练习册系列答案
相关题目
3.如图表示了绿色植物光合作用的主要过程,下列说法不正确的是( )


| A. | X是O2 | |
| B. | C6H12O6是有机物 | |
| C. | C6H12O6与X反应生成CO2和H2O属于置换反应 | |
| D. | 绿色植物通过光合作用,将太阳能转化成化学能 |
7.在AgNO3和Zn(NO3)2的混合溶液中,加入一定量的铁粉充分反应后,过滤、洗涤,将滤渣放入盐酸中有气泡产生,则滤渣成分的组成是( )
| A. | Fe、Ag | B. | Fe、Zn | C. | Zn、Ag | D. | Zn、Ag、Fe |
4.某研究性学习小组称取含NaCl的Na2CO3固体25g,将其配制成溶液,再向其中逐滴加入足量的7.3%的稀盐酸,使气体完全放出,共收集到 8.8g CO2气体.
(l)计算原固体中Na2CO3的质量分数和消耗稀盐酸的总质量.(写出计算过程)
(2)如表为研究性学习小组向上述配制的混合液中分三次逐滴加入(边加边振荡)稀盐酸后所记录的部分数据.经查阅资料知Na2CO3与HCl反应可以分两步进行:Na2CO3+HCl═NaCl+NaHCO3;NaHCO3+HCl═NaCl+H2O+CO2↑.
①请完成表格中未填的部分.
②根据表中数据在坐标系中画出CO2的质量(纵坐标)与所加入稀盐酸的质量(横坐标)的关系图.
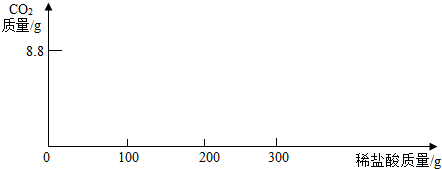
(l)计算原固体中Na2CO3的质量分数和消耗稀盐酸的总质量.(写出计算过程)
(2)如表为研究性学习小组向上述配制的混合液中分三次逐滴加入(边加边振荡)稀盐酸后所记录的部分数据.经查阅资料知Na2CO3与HCl反应可以分两步进行:Na2CO3+HCl═NaCl+NaHCO3;NaHCO3+HCl═NaCl+H2O+CO2↑.
①请完成表格中未填的部分.
| 实验次数 | 每次产生的CO2的质量/g |
| 第一次先逐滴滴加稀盐酸100g | 0 |
| 第二次再逐滴滴加稀盐酸100g | 8.8 |
| 第三次再逐滴滴加稀盐酸100g | 0 |

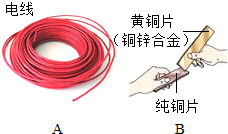 金属材料在生活、生产中应用十分广泛.
金属材料在生活、生产中应用十分广泛.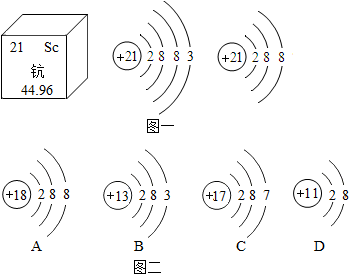
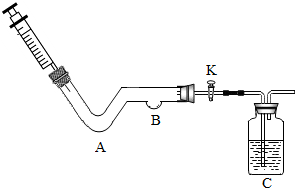 某化学小组同学利用如图所示装置进行实验.
某化学小组同学利用如图所示装置进行实验.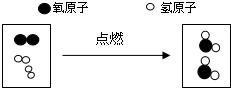 如图是某化学反应的微观示意图(表示氧原子,表示氢原子)
如图是某化学反应的微观示意图(表示氧原子,表示氢原子)