题目内容
19.高纯碳酸钙广泛应用医药、生活和生产中.由工业副产品氯化钙(含有氯化亚铁和氯化镁)制取高纯碳酸钙的流程如图1.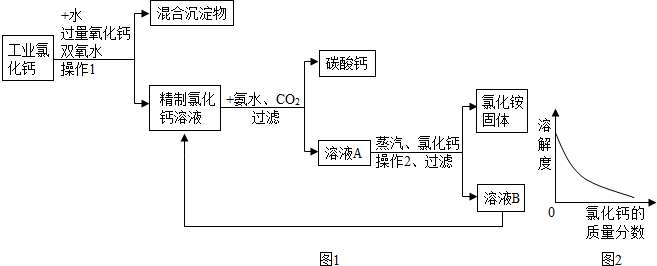
【查阅资料】①氯化铵受热会分解.
②室温下,氯化铵的溶解度随氯化钙的质量分数的变化关系如图2.
请回答下列问题:
(1)若在实验室完成操作1所需要的玻璃仪器有玻璃棒、烧杯和漏斗.
(2)氯化钙、氨气、二氧化碳和水制取碳酸钙,同时产生NH4Cl的反应化学方程式为CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.
(3)溶液B中的溶质是CaCl2和NH4Cl.
(4)溶液A经蒸发浓缩、操作2、加入氯化钙、过滤等过程方可获得氯化铵固体,操作2的名称是降温结晶,加入适量氯化钙使得氯化铵的溶解度减小(填“增大”、“减小”或“不变”).
分析 (1)根据操作1是过滤所用玻璃仪器解答;
(2)根据题目信息写出化学方程式;
(3)根据流程的反应解答;
(4)根据反应前后物质的状态回答.
解答 解:(1)操作1是过滤所用玻璃仪器有玻璃棒、烧杯、漏斗;
(2)氯化钙、氨气、二氧化碳和水制取碳酸钙,同时产生NH4Cl的反应化学方程式为CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl;
(3)氯化铵的溶解度随温度变化较大,所以应该用降温结晶法;向氯化铵溶液中逐渐加入氯化钙,氯化钙在溶液中的质量分数会逐渐增大,有图可知氯化铵的溶解度随氯化钙质量分数的增大而减小;从工艺流程图可看出,溶液B的主要成分是CaCl2和NH4Cl;
(4)溶液A经蒸发浓缩、操作2、加入氯化钙、过滤等过程方可获得氯化铵固体,操作2的名称是降温结晶,得到氯化铵固体,加入适量氯化钙使得氯化铵的溶解度减小结晶析出.
故答案为:
(1)漏斗; (2)CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl
(3)CaCl2和NH4Cl;(4)降温结晶 减小
点评 此题问题较多,涉及到的知识点也多,考查的知识点又比较零散.做此类题最关键的一点就是要有耐心,不要怕麻烦,一个小题一个小题的攻克它.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
10.下列有关碳和碳的氧化物的说法中错误的是( )
| A. | 石墨有良好的导电性,可用于制造干电池 | |
| B. | 干冰(固态二氧化碳)升华时吸热,可用于灭火,降低可燃物的着火点 | |
| C. | 金刚石是天然最硬的非金属单质,可制成钻石 | |
| D. | 一氧化碳都具有还原性,可用于冶铁 |
7.3月29日是“地球一小时”(Earth Hour)活动日,2015年度中国区主题是“能见蔚蓝”.作为一名中学生,下列做法不符合这一环保主题的是( )
| A. | 开发利用新能源 | B. | 草稿纸使用时要两面都用 | ||
| C. | 使用一次性木筷 | D. | 选择自行车作为出行工具 |
14.化学基本概念是学好化学的基础.对下列有关概念的认识正确的是( )
| A. | 原子是最小的微粒,不可再分 | |
| B. | 塑料、合成纤维和合成橡胶属于合成材料 | |
| C. | 均一、稳定的液体一定是溶液 | |
| D. | 中和反应是指能够生成盐和水的反应 |
11.下列相关事实用微观粒子的知识解释不正确的是( )
| 选项 | 事实 | 解释 |
| A | 酒精溶液是混合物 | 由不同种分子构成 |
| B | 水结冰后体积变大 | 水分子体积变大 |
| C | 墙内开花墙外可嗅到花香 | 分子不断运动 |
| D | 氢氧化钠溶液能导电 | 溶液中存在自由移动的Na+和OH- |
| A. | A | B. | B | C. | C | D. | D |
9.下列各组物质分别加入足量水中,固体能完全溶解,得到无色溶液的是( )
| A. | Na2CO3、NaCl、Na2SO4 | B. | FeCl3、NaOH、NaCl | ||
| C. | CuSO4、KCl、HCl | D. | Na2CO3、KCl、CaCl2 |
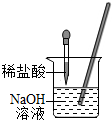 化学兴趣小组的同学用图所示装置进行中和反应实验,请你参与下列探究:为确定稀盐酸与氢氧化钠溶液是否刚好完全中和,小华取出一定量反应后的溶液于一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论.
化学兴趣小组的同学用图所示装置进行中和反应实验,请你参与下列探究:为确定稀盐酸与氢氧化钠溶液是否刚好完全中和,小华取出一定量反应后的溶液于一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论.
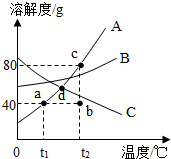 如图是常见固体物质的溶解度曲线,根据图示回答:
如图是常见固体物质的溶解度曲线,根据图示回答: