题目内容
下列图象正确反映对应的变化关系的是( )
A、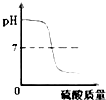 向一定量的稀硫酸中滴加氢氧化钠溶液至过量 |
B、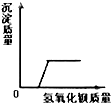 向一定量的硫酸和硫酸镁混合溶液中滴加氢氧化钡溶液 |
C、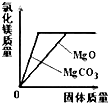 将足量碳酸镁和氧化镁固体分别加入相同质量、相同质量分数的稀盐酸中 |
D、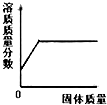 在一定温度下,向不饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌 |
考点:中和反应及其应用,溶质的质量分数,酸的化学性质,碱的化学性质
专题:元素化合物知识型
分析:A、向一定量的稀硫酸中滴加氢氧化钠溶液至过量的过程中,是酸不断消耗酸性不断减弱,恰好反应时PH=7,直至过量PH大于7.
B、向一定量的硫酸和硫酸镁混合溶液中滴加氢氧化钡溶,一开始就会生成沉淀.
C、将足量碳酸镁和氧化镁固体分别加入相同质量、相同质量分数的稀盐酸时,生成等量的氯化镁,反应因氧化镁的含镁量较高消耗氧化镁的质量小于碳酸镁的质量.
D、不饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌时溶液的溶质质量分数不断升高直至饱和.
B、向一定量的硫酸和硫酸镁混合溶液中滴加氢氧化钡溶,一开始就会生成沉淀.
C、将足量碳酸镁和氧化镁固体分别加入相同质量、相同质量分数的稀盐酸时,生成等量的氯化镁,反应因氧化镁的含镁量较高消耗氧化镁的质量小于碳酸镁的质量.
D、不饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌时溶液的溶质质量分数不断升高直至饱和.
解答:解:A、稀硫酸呈酸性,故起初溶液的pH小于7,但随着氢氧化钠溶液的加入,会发生酸碱中和反应,使稀硫酸逐渐减少,酸性渐弱,两者恰好完全反应时溶液呈中性pH=7,继续加入氢氧化钠则碱加量,溶液呈碱性,图象相反,故选项A错误;
B、硫酸和硫酸镁都能喝氢氧化钡溶液反应生成白色的硫酸钡沉淀,所以反应开始就会产生沉淀,即沉淀的曲线的起点为原点,故选项B错误.
C、将足量碳酸镁和氧化镁固体分别加入相同质量、相同质量分数的稀盐酸时,由于产生的氯化镁取决于盐酸,而盐酸中的氯离子是相等的,所以生成的氯化镁也相等.但是由于碳酸镁的相对分子质量大,所以应该消耗的碳酸镁固体多,氧化镁少,故选项C错误.
D、不饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌时溶液的溶质质量分数不断升高直至饱和,溶质质量分数不断变大最终会变成一条水平直线.故选项D正确.
故选:D
B、硫酸和硫酸镁都能喝氢氧化钡溶液反应生成白色的硫酸钡沉淀,所以反应开始就会产生沉淀,即沉淀的曲线的起点为原点,故选项B错误.
C、将足量碳酸镁和氧化镁固体分别加入相同质量、相同质量分数的稀盐酸时,由于产生的氯化镁取决于盐酸,而盐酸中的氯离子是相等的,所以生成的氯化镁也相等.但是由于碳酸镁的相对分子质量大,所以应该消耗的碳酸镁固体多,氧化镁少,故选项C错误.
D、不饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌时溶液的溶质质量分数不断升高直至饱和,溶质质量分数不断变大最终会变成一条水平直线.故选项D正确.
故选:D
点评:此题是化学反应与图象知识的考查题,结合反应的过程与图象情况的走势联系起来是解题的关键所在.

练习册系列答案
相关题目
一位学生要用托盘天平称取2.5g药品,在称量中发现指针向左偏转,这时他应该( )
| A、增加药品 | B、减少药品 |
| C、移动游码 | D、向右盘中加砝码 |
正确的实验操作是实验成功的保证,下列实验操作正确的是( )
A、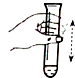 上下振荡试管 |
B、 读取液体体积 |
C、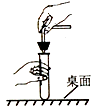 塞紧橡胶塞 |
D、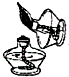 点燃酒精灯 |
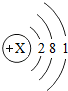 ,则X的值为
,则X的值为