题目内容
探秘海滩上的物质
在海滩上,你能看到各种各样的物质,除海洋生物外,最常见的有海沙,贝壳和海水,虽然他们性质与用途各异,但从元素组成的角度看,这些物质都是由氧、硅、氟、钾、钙等有限的几种元素组成的.
原子是构成物质的“基石”,一种原子,可以构成 最常见的单质,但更多的是和其他原子结合成各种化合物,请回答:
最常见的单质,但更多的是和其他原子结合成各种化合物,请回答:
(1)从化学的视角认识物质
①海沙是由石英和贝壳的碎片组成,石英的主要成分是(用化学符号表示,下同) ,贝壳的主要成分是 ;
②请写出一种同时符合下列两个条件的化合物的名称或 化学式
化学式
(Ⅰ)由氧、硅、氟、钾、钙五种元素中的三种组成;
(Ⅱ)根据分类,与①中两种物质的主要成分类别不同
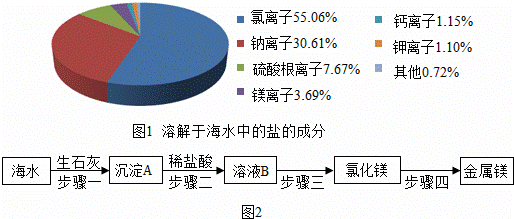
③海水中含有多种无机盐,各离子的含量如图1所示,其中由硫酸根离子和镁离子构成的化学式是 ,假设海水中无机盐的含量为3.8%,钾离子全部以氯化钾的形式存在,则Wg海水中含有氯化钾质量的计算公式为 .
④各地海水中盐的含量并不完全相同,在接近入海口处,海水中盐的含量较低,原因是 .
⑤食用微钠盐可预防高血压,低碘盐是在氯化钠中加了氯化钾,氯化钾除了有咸味外,还带有苦味,从物质构成的角度看,氯化钾有苦味可能是 造成的.
(2)用化学的方法改造物质
海水中含有丰富的镁元素,目前工业上绝大多数的金属镁是从海水中提取的,其生产流程如图2:
①步骤一中发生反应的化学方程式为 , .
②上述生产流程中发生的反应,没有涉及到的基本反应类型是 .
③在步骤一中,分离出沉淀A的方法是 .
| 化学式的书写及意义;生石灰的性质与用途;盐 | |
| 专题: | 化学式的计算;化学用语和质量守恒定律;常见的盐 化学肥料. |
| 分析: | (1)①熟记常见物质的主要成分;②根据提供的元素和物质的类别来确定物质的化学式;③根据溶质的质量=溶液的质量×溶液中溶质的质量分数来计算;④从入海的河水含盐量较低来分析;⑤从氯化钠和氯化钾的构成异同点来分析; (2)①当将生石灰放入海水中,氧化钙先与水反应生成氢氧化钙,然后氢氧化钙再与氯化镁反应; ②明确每一步中发生的化学反应及其类型就能顺利解答; ③将固体与液体分离开的方法是过滤. |
| 解答: | 解:(1)①石英砂的主要成分是二氧化硅,贝壳的主要成分是碳酸钙;故填:SiO2 ②上述两种物质分属于氧化物和盐,根据提供的元素可以组成的符合两个条件的是氢氧化 ③镁离子带2个单位的正电荷,硫酸根离子带2个单位的负电荷,故硫酸镁的化学式为:MgSO4,Wg海水中含有钾离子的质量为:Wg×3.8%×1.10%,那么氯化钾的质量为 ④在河流的入海口处,有大量的河水注入海洋,相对于海水来讲,注入海洋的河流属于淡水.所以注入海洋的河水,等于是增加了入海口处海水中的水(溶剂),造成该处海水盐的浓度降低;故填:河水中的淡水将海水中的盐分稀释; ⑤氯化钠是由钠离子和氯离子构成的,没有苦味,氯化钾是由钾离子和氯离子构成的,有苦味,据此分析可能是钾离子导致氯化钾具有苦味的;故填:钾离子; (2)①在步骤一中:氧化钙与水反应生成氢氧化钙,然后氢氧化钙与氯化镁反应生成氯化钙和氢氧化镁白色沉淀;故填:CaO+H2O=Ca(OH)2;Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2; ② ③通过过滤可以把沉淀从溶液中分离出来.故填:过滤. |
| 点评: | 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,有助于提高观察实验、进行实验的能力. |

 全能测控一本好卷系列答案
全能测控一本好卷系列答案竹子是“有节、中空、四季常绿”的植物(如图所示)。同学们对竹子中的气体成分展开了探究,测定其成分。(10分)
(1)收集竹子中的气体。
小华提出:将一节竹子浸没在水中,在竹子上钻孔,用排水法收集气体。
小刚提出:可用注射器从竹子中抽取气体。
大家认为两人的想法都可行,于是分为A、B两组,在相同的条件下,A组采用小华的取气方法,B组采用小刚的取气方法,分别完成下面的实验。
(2)检验气体中是否含有二氧化碳气体。
| 实验步骤 | 实验现象 | 实验结论及解释 |
| 向所取气体中加入
|
| 有二氧化碳,化学方程式为: |
(3)测定气体中氧气含量。
【查阅资料】红磷的着火点为240℃,白磷的着火点为40℃。
【设计实验】同学们设计了如下图所示的方案一和方案二来测定氧气含量。

【进行实验】按上述两个方案 进行多次实验。
进行多次实验。
【反思与评价】
①实验中磷的量应为足量,目的是  ;
;
②两个方案的实验测定结果不同,测定结果比较准确的是方案  ,原因是 。
,原因是 。
③经过A、B两组同学的实验,A组测得的含氧量总是大于B组的,你认为 原因是
原因是
。
下列现象或事实,可用金属活动性作出解释的是( )
①黄铜(铜锌合金)外观与黄金相似,但可将两者放入稀盐酸中加以区别
②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强
③用硫酸铜、石灰水配置农药波尔多液时,不能用铁制容器.
|
| A. | ② | B. | ①③ | C. | ②③ | D. | ①②③ |
下列过程一定发生化学变化的是( )
|
| A. | 萝卜风干 | B. | 苹果冷藏 | C. | 葡萄酿酒 | D. | 甘蔗榨汁 |
铁钉在下列哪种情况下最容易生锈( )
|
| A. | 干燥的空气中 | B. | 潮湿的空气中 |
|
| C. | 浸入植物油中 | D. | 干燥致密的土壤中 |
一些物质在常温下的近似pH如下表:
| 物质 | 血浆 | 胃液 | 正常雨水 | 葡萄汁 |
| PH | 7.35~7.45 | 0.9~1.5 | ≈5.6 | 3.5~4.5 |
下列有关上述四种物质的说法中正确的是( )
|
| A. | 只有葡萄汁显酸性 | B. | 只有血浆显碱性 |
|
| C. | 正常雨水显中 | D. | 胃酸过多的人应多饮用葡萄汁 |
 的化学性质;化合物中某元素的质量计算;反应类型的判定;书写化学方程式、文字表达式、电离方程式;对海洋资源的合理开发与利
的化学性质;化合物中某元素的质量计算;反应类型的判定;书写化学方程式、文字表达式、电离方程式;对海洋资源的合理开发与利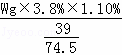 .故填:MgSO4;
.故填:MgSO4;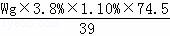 ;
; 的是
的是 
 性
性