题目内容
19. 手机在人们的生活中使用广泛,如图是充电或连接用的数据线.
手机在人们的生活中使用广泛,如图是充电或连接用的数据线.(1)所标物质中属于金属单质的是铁或铜,属于有机合成材料的是塑料.
(2)数据线的铁制插头在日常潮湿的空气中会生锈,铁生锈是一个复杂的过程,铁锈的主要成分是Fe2O3•xH2O,由此可知参加反应的是铁、氧气和水.
(3)写出只有一步反应表示铁比铜活泼的化学方程式:Fe+CuSO4=Cu+FeSO4.
分析 (1)根据已有的物质的类别解答;
(2)根据铁生锈的条件解答;
(3)根据铁与硫酸铜反应的知识进行分析解答即可.
解答 解:(1)据图可以看出,铁和铜是金属单质,塑料属于有机合成材料,故填:铁或铜,塑料;
(2)铁与水和氧气并存时易生锈,故填:水;
(3)铁与硫酸铜反应生成硫酸亚铁和铜,故填:Fe+CuSO4=Cu+FeSO4;
答案:(1)铁或铜;塑料;(2)水;(3)Fe+CuSO4=Cu+FeSO4.
点评 本题考查的是金属材料的有关应用和性质的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
9.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热易分解,某兴趣小组同学对其分解产物进行如下探究:
【猜想】小组同学们提出如表三种猜想
你认为合理的猜想是3.
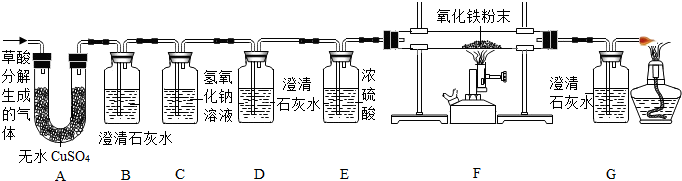
【设计实验】为了检验草酸分解的产物,该小组同学经过讨论设计了如图所示装置,并进行了实验(部分夹持仪器已略去).(提示:无水硫酸铜遇水会变为蓝色)
【实验探究】
(1)实验过程中,观察到A中无水硫酸铜变蓝,B中澄清石灰水变浑浊,证明草酸分解产生了H2O和CO2.
(2)C中发生反应的化学方程式CO2+2NaOH═Na2CO3+H2O.设计 D装置的作用是检验CO2是否已被完全除去.
(3)若实验过程中观察到D中澄清石灰水未变浑浊,F中固体由黑色变为红色,G中澄清石灰水变浑浊现象.即可证明生成物 中有CO气体.
【实验结论】若猜想3正确,则草酸受热分解的化学方程式为H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$H2O+CO2↑+CO↑.
【猜想】小组同学们提出如表三种猜想
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO和H2O | 只有CO2和H2O | CO、CO2和H2O |
【设计实验】为了检验草酸分解的产物,该小组同学经过讨论设计了如图所示装置,并进行了实验(部分夹持仪器已略去).(提示:无水硫酸铜遇水会变为蓝色)

【实验探究】
(1)实验过程中,观察到A中无水硫酸铜变蓝,B中澄清石灰水变浑浊,证明草酸分解产生了H2O和CO2.
(2)C中发生反应的化学方程式CO2+2NaOH═Na2CO3+H2O.设计 D装置的作用是检验CO2是否已被完全除去.
(3)若实验过程中观察到D中澄清石灰水未变浑浊,F中固体由黑色变为红色,G中澄清石灰水变浑浊现象.即可证明生成物 中有CO气体.
【实验结论】若猜想3正确,则草酸受热分解的化学方程式为H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$H2O+CO2↑+CO↑.
10. 钛合金因具有强度高、耐腐蚀性好、耐热性高等特点而被广泛用于各个领域.在元素周期表中位于第4周期的钛元素有关信息如图所示,下列说法正确的是( )
钛合金因具有强度高、耐腐蚀性好、耐热性高等特点而被广泛用于各个领域.在元素周期表中位于第4周期的钛元素有关信息如图所示,下列说法正确的是( )
 钛合金因具有强度高、耐腐蚀性好、耐热性高等特点而被广泛用于各个领域.在元素周期表中位于第4周期的钛元素有关信息如图所示,下列说法正确的是( )
钛合金因具有强度高、耐腐蚀性好、耐热性高等特点而被广泛用于各个领域.在元素周期表中位于第4周期的钛元素有关信息如图所示,下列说法正确的是( )| A. | 钛元素为非金属元素 | B. | 钛原子核外电子数为26 | ||
| C. | 钛原子的相对原子质量为47.867g | D. | 钛原子的核外有四个电子层 |
7.下列有关对质量守恒定律的理解,正确的是( )
| A. | 将5g氯化钠完全溶解在95g水中,溶液的质量为100g | |
| B. | 2g氢气和8g氧气混合点燃,生成水的质量是9g | |
| C. | 镁条燃烧后质量增加,不遵循质量守恒定律 | |
| D. | 将5g铁和5g铜混合加热后,物质的总质量为10g |
14.安徽省实施“清水蓝天”工程以来,环境质量得到显著提升.如图行为不利于“清水蓝天”工程实施的是
( )
( )
| A. |  分类回收垃圾 | B. |  使用太阳能路灯 | ||
| C. |  开发氢能源电池客车 | D. |  直接排放废水 |
 20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图1所示的现象.
20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图1所示的现象.