题目内容
15.某校九年级化学实验操作技能考查中,小华抽到的试题是“水的净化”,请你与小华一起实验,并回答下列问题.(1)过滤操作中用到的玻璃仪器有漏斗、玻璃棒和烧杯烧杯,其中玻璃棒的作用是引流.
(2)小华准备按如图1所示的装置进行操作时,发现装置存在一处明显错误,该错误是漏斗的下端没有紧靠烧杯内壁,漏斗的低端没有紧靠烧杯内壁纠正错误后,接下来的过滤操作可除去水样中的不溶性不溶性(填“可溶性”或“不溶性”)杂质.若要除去其中的异味,应用活性炭(填名称)
(3)小华即将浑浊的水样过滤后,得到的水仍浑浊,其原因可能是液面高于滤纸边缘液面高于滤(写出一点即可),然后小华进行了有效处理,使水样变的澄清透明.在生活中,要想将硬水转化为软水,方法是加热煮沸.
(4)将原水处理成自来水需要加入消毒剂.其中用液氯消毒时发生反应的微观过程如图2:
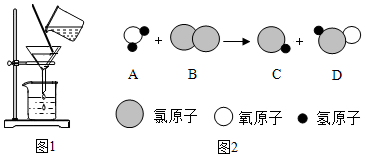
上述物质中属于单质的是Cl2(填化学式),该反应的化学方程式为:Cl2+H2O=HCl+HClO D物质中氯元素的化合价为+1.
分析 (1)根据过滤操作用到的玻璃仪器进行解答,该操作中玻璃棒的作用是引流解答;
(2)根据过滤操作中注意事项及过滤的原理进行解答;
(3)过滤后滤液仍浑浊的原因可能是:液面高于滤纸边缘或滤纸破损、仪器不干净;加热能将水中的可溶性钙镁化合物转化为不溶性钙镁化合物解答;
(4)根据氯气和水反应生成盐酸和次氯酸,根据正负化合价的代数和为零求元素的化合价解答.
解答 解:
(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒、漏斗,该操作中玻璃棒的作用是引流;故答案为:烧杯;引流.
(2)过滤时要注意一贴、二低、三靠,用玻璃棒引流,而图示漏斗的下端没有紧靠烧杯内壁;过滤是把不溶于液体的固体物质跟液体分离开来的一种混合物分离的方法,常用来除去水中不溶性杂质;利用活性炭的吸附性,可以除去水中的异味;故答案为:漏斗的下端没有紧靠烧杯内壁;不溶性;活性炭;
(3)过滤后滤液仍浑浊的原因可能是:液面高于滤纸边缘或滤纸破损、仪器不干净;加热能将水中的可溶性钙镁化合物转化为不溶性钙镁化合物,从而实现硬水软化;故答案为:液面高于滤纸边缘,加热煮沸.
(4)由同种元素组成的纯净物是单质;上述物质中属于单质的是B氯气;氯气和水反应生成盐酸和次氯酸,该反应的化学方程式为:Cl2+H2O=HCl+HClO;根据正负化合价的代数和为零,设氯元素的化合价为x,+1+x+(-2)=0 x=+1
答案:
(1)烧杯 引流
(2)漏斗的下端没有紧靠烧杯内壁;不溶性;活性炭;
(3)液面高于滤纸边缘 加热煮沸
(4)Cl2 Cl2+H2O=HCl+HClO;+1;
点评 本题主要考查了过滤的原理、所用仪器及运用和对实验结果的分析等知识,培养了学生分析问题的能力.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
1.下列说法或做法正确的是( )
| A. | 在人群密集的地方,不要停留太长时间以防止中毒 | |
| B. | 不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上氢氧化钠溶液 | |
| C. | 在日常生活中用蒸馏的方法将硬水软化 | |
| D. | 天然气泄漏报警器应安装在灶台的上方 |
20.今年央视“3•15”特别节目曝光,某品牌肉制品中含有毒物质瘦肉精.某种瘦肉精的化学式为C10H19Cl3N2O,下列有关该瘦肉精的说法中正确的是( )
| A. | 该瘦肉精由10个碳原子、19个氢原子、3个氯原子、2个氮原子和1个氧原子构成 | |
| B. | 该瘦肉精分子中含有氮分子 | |
| C. | 该瘦肉精由碳、氢、氯、氮、氧五种元素组成 | |
| D. | 该瘦肉精是混合物 |
7.下列化肥中,属于复合肥的是( )
| A. | NH4Cl | B. | NH4NO3 | C. | KNO3 | D. | Ca3(PO4)2 |
 实验室现有一种含有氯化钠的纯碱固体样品.某化学兴趣小组的同学在老师的指导下,利用如图所示装置(部分固定装置已略去)进行实验,测定其中纯碱的含量,并证实二氧化碳能与氢氧化钠发生化学反应.已知,该装置气密性良好,氢氧化钠溶液过量.
实验室现有一种含有氯化钠的纯碱固体样品.某化学兴趣小组的同学在老师的指导下,利用如图所示装置(部分固定装置已略去)进行实验,测定其中纯碱的含量,并证实二氧化碳能与氢氧化钠发生化学反应.已知,该装置气密性良好,氢氧化钠溶液过量. 根据图示回答:白磷的着火点约为40℃,红磷的着火点约为240℃,酒精灯的火焰约为 500℃.在铜片上将烧杯、白磷(A、C点),红磷(D点)、石灰石块(B点)摆放好,再点燃酒精灯加热片刻,先发生燃烧现象的是C点,不会发生燃烧现象的是D点,由现象A、C得到的燃烧条件是可燃物需要与氧气接触;由现象B、C得到的燃烧条件是物质需要具有可燃性;根据C、A确定的燃烧的条件,请举出一种生活中常见的灭火方法油锅着火盖上锅盖.联系所学化学知识,请你指出本实验装置不足之处:生成的五氧化二磷挥发到空气中造成污染.
根据图示回答:白磷的着火点约为40℃,红磷的着火点约为240℃,酒精灯的火焰约为 500℃.在铜片上将烧杯、白磷(A、C点),红磷(D点)、石灰石块(B点)摆放好,再点燃酒精灯加热片刻,先发生燃烧现象的是C点,不会发生燃烧现象的是D点,由现象A、C得到的燃烧条件是可燃物需要与氧气接触;由现象B、C得到的燃烧条件是物质需要具有可燃性;根据C、A确定的燃烧的条件,请举出一种生活中常见的灭火方法油锅着火盖上锅盖.联系所学化学知识,请你指出本实验装置不足之处:生成的五氧化二磷挥发到空气中造成污染.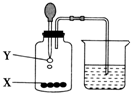 如图所示,瓶中X为固体,当把滴管内的液体Y滴入瓶中时,伸入烧杯中的导气管口出现气泡的是A
如图所示,瓶中X为固体,当把滴管内的液体Y滴入瓶中时,伸入烧杯中的导气管口出现气泡的是A