题目内容
13.有CO、CO2和N2组成的混合物,已知混合物中碳元素的质量分数为24%,则N2的质量分数可能是( )| A. | 8% | B. | 12% | C. | 30% | D. | 44% |
分析 设该混合气体的质量为100g.则混合气体中含碳24克,假设全部是二氧化碳,求出此时氮气的质量,假设全部是一氧化碳,求出此时氮气的质量,氮气的质量应在这两个值之间.
解答 解:设该混合气体的质量为100g.则混合气体中含碳元素24g,假设全部来自于二氧化碳,则二氧化碳的质量为:24g÷$\frac{12}{44}×100%$=88g,则氮气为:100g-88g=
12g;假设全部来自于一氧化碳,则一氧化碳的质量为:24g÷$\frac{12}{28}×100%$=56g,求出此时氮气的质量为100g-56g=44克,氮气的质量应在这两个值之间.故氮气的质量分数也是在12%到44%之间即可.
故选:C.
点评 本题是一道考查混合物质中根据某元素的质量分数来求的另外几种物质或者元素的质量分数,方法有多种,但可以用排除法做类似的题目;难度较大,培养学生的创新和逆向思维能力.

练习册系列答案
相关题目
4.有关物质的量,说法错误的是( )
| A. | 物质的量是联系宏观世界和微观粒子的桥梁 | |
| B. | 物质的摩尔质量在数值上等于式量或相对原子质量 | |
| C. | 摩尔是国际单位制中七个基本物理量之一 | |
| D. | 1mol任何物质都含有约6.02×1023个微粒 |
1.实验室中如图所示药品存放规范的是( )
| A. |  氧气 | B. |  石灰水 | C. |  食盐 | D. | 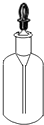 稀硫酸 |
8.富氧炼钢用的富氧空气中氧气含量高于普通空气,富氧空气中氧气与其他气体的体积比可能是( )
| A. | 1:3 | B. | 1:4 | C. | 1:5 | D. | 21:79 |
18.某学习小组用木炭还原氧化铜,反应中固体质量随时间变化的数据见表.
(1)反应生成的气体质量8.8g.
(2)计算被还原的氧化铜的物质的量.(根据化学方程式计算)0.4mol.
| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 38.0 | 33.6 | 29.2 | 29.2 |
(2)计算被还原的氧化铜的物质的量.(根据化学方程式计算)0.4mol.
3.下列实验现象描述正确的是( )
| A. | 硫在空气中燃烧产生强烈的蓝紫色火焰 | |
| B. | 铁丝在氧气中燃烧生成四氧化三铁 | |
| C. | 木炭在氧气中燃烧产生红色火焰 | |
| D. | 白磷在空气中燃烧产生大量的白烟 |