题目内容
如表是硝酸钾和氯化钠在不同温度时的溶解度:
(1)从上表可以看出,影响物质的溶解度的因素有(填一种)
(2)30℃时氯化钠的溶解度是 ,该温度下 (填“能”或“不能”) 配制出45.8%的硝酸钾溶液.
(3)根据上表提供的数据可绘制出两物质的溶解度曲线,请推测两曲线交点的温度范围是 .
(4)70℃时,分别用100克水配制硝酸钾、氯化钠的饱和溶液,然后降温至20.下列说法的是 .
A、20℃时,得到的均为饱和溶液
B、析出的硝酸钾晶体比氯化钠晶体多
C、20℃时,硝酸钾溶液的浓度大于氯化钠溶液的浓度.
| 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
| 溶解度 | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | |
(2)30℃时氯化钠的溶解度是
(3)根据上表提供的数据可绘制出两物质的溶解度曲线,请推测两曲线交点的温度范围是
(4)70℃时,分别用100克水配制硝酸钾、氯化钠的饱和溶液,然后降温至20.下列说法的是
A、20℃时,得到的均为饱和溶液
B、析出的硝酸钾晶体比氯化钠晶体多
C、20℃时,硝酸钾溶液的浓度大于氯化钠溶液的浓度.
考点:固体溶解度的影响因素,饱和溶液和不饱和溶液,固体溶解度的概念,晶体和结晶的概念与现象
专题:溶液、浊液与溶解度
分析:(1)根据表中数据可知影响物质溶解度的因素有温度、溶质的种类;
(2)根据30℃时氯化钠的溶解度36.3g以及30℃时硝酸钾的溶解度45.8g进行解答;
(3)根据硝酸钾和氯化钠溶解度相同的温度既是判断该段中溶解度的数值是否存在相等的可能进行解答;
(4)根据硝酸钾和氯化钠的溶解度进行解答.
(2)根据30℃时氯化钠的溶解度36.3g以及30℃时硝酸钾的溶解度45.8g进行解答;
(3)根据硝酸钾和氯化钠溶解度相同的温度既是判断该段中溶解度的数值是否存在相等的可能进行解答;
(4)根据硝酸钾和氯化钠的溶解度进行解答.
解答:解:(1)根据表中数据可以看出:不同温度下两物质的溶解度不同,溶质不同,溶解度也不同,由此可知影响溶解度的因素有温度、溶质的种类;
(2)30℃时氯化钠的溶解度36.3g;30℃时硝酸钾的溶解度45.8g,该温度下饱和溶液的质量分数为=
×100%=31.4%,所以该温度下 不能配制出45.8%的硝酸钾溶液;
(3)硝酸钾和氯化钠溶解度相同的温度既是判断该段中溶解度的数值是否存在相等的可能,经分析知在20~40℃时这两种物质存在溶解度相同的可能;
(4)A、硝酸钾和氯化钠的溶解度都随温度的降低而减小,所以20℃时,得到的均为饱和溶液,故正确;
B、硝酸钾的溶解度受温度的影响变化较大,所以析出的硝酸钾晶体比氯化钠晶体多,故正确;
C、20℃时,氯化钠的溶解度大于硝酸钾,所以20℃时硝酸钾溶液的浓度小于氯化钠溶液的浓度,故错误.
故答案为:(1)温度;(2)36.3g;不能;(3)20~40℃;(4)AB.
(2)30℃时氯化钠的溶解度36.3g;30℃时硝酸钾的溶解度45.8g,该温度下饱和溶液的质量分数为=
| 45.8g |
| 45.8g+100g |
(3)硝酸钾和氯化钠溶解度相同的温度既是判断该段中溶解度的数值是否存在相等的可能,经分析知在20~40℃时这两种物质存在溶解度相同的可能;
(4)A、硝酸钾和氯化钠的溶解度都随温度的降低而减小,所以20℃时,得到的均为饱和溶液,故正确;
B、硝酸钾的溶解度受温度的影响变化较大,所以析出的硝酸钾晶体比氯化钠晶体多,故正确;
C、20℃时,氯化钠的溶解度大于硝酸钾,所以20℃时硝酸钾溶液的浓度小于氯化钠溶液的浓度,故错误.
故答案为:(1)温度;(2)36.3g;不能;(3)20~40℃;(4)AB.
点评:此题是溶解度知识的具体应用,对学生深入理解溶解度的概念有一定帮助,同时也复习了有关混合物分离的一些常识性的基础知识.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、KNO3、NH4H2PO4、NH4NO3都是复合肥 |
| B、糖类、油脂、蛋白质都是供能的营养物质 |
| C、煤、石油、天然气都是不可再生能源 |
| D、新鲜的水果、蔬菜都含有人体所需的不同的维生素 |
下列常见物质中,属于纯净物的是( )
| A、18K黄金 | B、加碘食盐 |
| C、车用乙醇汽油 | D、蒸馏水 |
 生产生活中,钙元素的存在非常广泛.
生产生活中,钙元素的存在非常广泛.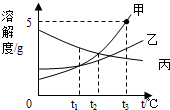 如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
 ”和“
”和“ ”分子个数比是
”分子个数比是