题目内容
13.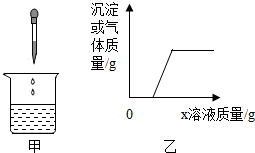 向烧杯中逐滴加入x溶液至过量(图甲),生成沉淀或气体的质量与加入x溶液的质量关系符合图乙的是( )
向烧杯中逐滴加入x溶液至过量(图甲),生成沉淀或气体的质量与加入x溶液的质量关系符合图乙的是( )| 烧杯中的物质 | x溶液 | |
| ① | 稀盐酸和硫酸铜 | 烧碱 |
| ② | 稀硫酸和稀盐酸 | 氯化钡 |
| ③ | 镁铝合金 | 稀盐酸 |
| ④ | 氯化钠和碳酸钠溶液 | 稀盐酸 |
| A. | ①④ | B. | ①③④ | C. | ①② | D. | ① |
分析 解答本题首先分析图象的意义是随着乙的不断加入,反应开始没有气体或沉淀生成,然后气体或沉淀逐渐增加,其次将四个反应的化学反应原理逐一分析,分析气体或沉淀的生成与x溶液的关系,最后和图象对比可完成解答.
解答 解:①氢氧化钠能和硫酸铜反应生成氢氧化铜沉淀,氢氧化铜能和盐酸反应生成氯化铜和水,开始没有沉淀出现,当盐酸消耗完后才出现沉淀.故正确;
②稀硫酸和氯化钡溶液反应生成难溶于水且难溶于酸的沉淀,即将氯化钡溶液滴加入稀硫酸和稀盐酸的混合溶液中马上产生沉淀,即生成沉淀的起点为原点,故错误.
③镁铝都能和盐酸反应生成气体,且只要接触就能产生氢气,即生成气体的起点为原点,故错误;
④氯化钠不能和稀盐酸反应,而碳酸氢钠能够和稀盐酸反应生成二氧化碳气体,该反应常温下即可反应生成气体,即生成气体的起点为原点,故错误.
故选D.
点评 本题是图象和化学知识相结合的题型,涉及知识点较多.要求学生有将图象信息转换为化学信息的能力,同时对化学知识必须十分熟练,才可能快速解题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
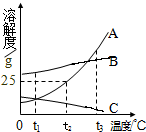
8.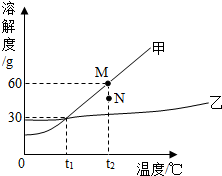 如图为甲﹑乙两物质的溶解度曲线.下列说法不正确的是( )
如图为甲﹑乙两物质的溶解度曲线.下列说法不正确的是( )
 如图为甲﹑乙两物质的溶解度曲线.下列说法不正确的是( )
如图为甲﹑乙两物质的溶解度曲线.下列说法不正确的是( )| A. | 甲的溶解度受温度变化影响比乙大 | |
| B. | t1℃时,甲、乙两物质饱和溶液中溶质的质量分数相同 | |
| C. | 要使组成在N点的甲溶液转变为M点的甲溶液,可以采用升高温度的方法 | |
| D. | 乙采用蒸发溶剂的方法得到乙晶体 |
5.下列化学方程式不正确的是( )
| A. | Na2CO3+2HCl=2NaCl+H2O+CO2↑ | B. | NaOH+HCl=NaCl+H2O | ||
| C. | Fe+CuSO4=FeSO4+Cu | D. | CH4+O2$\frac{\underline{\;点燃\;}}{\;}$CO2+H2O |
2.下列物质敞口防止在空气中,质量发生变化与空气的成分无关的是( )
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 苛性钠 | D. | 铝丝 |
3.如表是Ca(OH)2和NaNO3的溶解度数据,请回答下列问题.
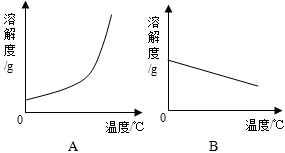
(1)依据如表数据,绘制Ca(OH)2和NaNO3的溶解度曲线,图中能表示NaNO3溶解度曲线的是A(填“A”或“B”).
(2)要向把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有①②⑤(填序号).
①蒸发水 ②升高温度 ③降低温度 ④加入水 ⑤加入氢氧化钙
(3)现有60℃时含Ca(OH)2和NaNO3两种溶质的饱和溶液,若要得到纯净的NaNO3晶体,应采取的物理方法是降温结晶,过滤.
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量的CaO后恢复到20℃,得到乙溶液,溶液中溶质的质量分数的关系为甲=乙(填“>”、“<”或“=”).
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaNO3 | 31 | 91 | 111 | 129 | 313 | 336 | |

(1)依据如表数据,绘制Ca(OH)2和NaNO3的溶解度曲线,图中能表示NaNO3溶解度曲线的是A(填“A”或“B”).
(2)要向把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有①②⑤(填序号).
①蒸发水 ②升高温度 ③降低温度 ④加入水 ⑤加入氢氧化钙
(3)现有60℃时含Ca(OH)2和NaNO3两种溶质的饱和溶液,若要得到纯净的NaNO3晶体,应采取的物理方法是降温结晶,过滤.
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量的CaO后恢复到20℃,得到乙溶液,溶液中溶质的质量分数的关系为甲=乙(填“>”、“<”或“=”).
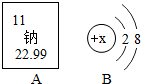 如图A是钠元素在元素周期表中的相关信息,图B是该元素形成的一种粒子的结构示意图.
如图A是钠元素在元素周期表中的相关信息,图B是该元素形成的一种粒子的结构示意图.