题目内容
10.过氧化氢溶液常用于实验室制取氧气.可供选择的仪器或装置如图1所示.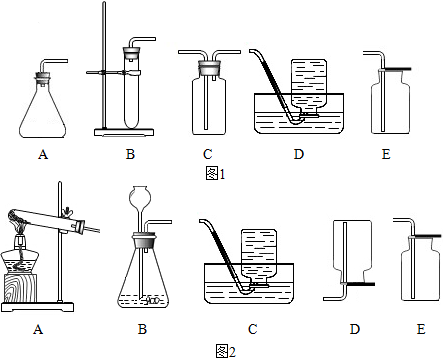
(1)要收集干燥的氧气,整套装置的连接顺序为ACE(选填字母A~E),装置C盛放的液体是浓硫酸.
(2)过氧化氢溶液制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,MnO2可以连续反应使用,理由是二氧化锰是催化剂,反应前后质量和化学性质都不变.
(3)根据化学方程式计算获得的氧气理论值总是比实际实验操作收集到气体的数值大(若装置不漏气且实验操作正确),原因是生成的氧气有少量溶解在水中.
(4)生产火箭燃料的工业废水中含有少量偏二甲肼X,可用双氧水处理排污,反应的化学方程式为:X+8H2O2═2CO2↑+N2↑+12H2O,则X的化学式为C2H8N2.
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,可供选择的仪器或装置如图2所示,常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,NH3极易溶于水,其水溶液呈碱性,现选择合适的装置来制取并收集NH3,应该选择的发生装置是A,收集装置是D,若用湿润的红色石蕊试纸来检验NH3,产生的现象是变蓝.
分析 (1)收集干燥的氧气,不能使用排水法收集,为除去混在气体中的水,需要使用干燥剂对气体进行干燥处理;
(2)反应中的二氧化锰是反应的催化剂,在反应前后其质量和化学性质不变,仍可以继续使用
(3)生成的氧气有少量溶解在水中,因此根据化学方程式计算获得的氧气理论值总是比实际实验操作收集到气体的数值大;
(4)利用反应的化学方程式,根据化学变化前后原子种类、数目不变,推导出偏二甲肼的分子构成,写出其化学式;
(5)发生装置主要由反应物的状态和反应条件决定;收集装置主要由气体的密度和溶水性决定.
解答 解:(1)收集干燥的氧气,可把气体能过装置浓硫酸的装置C后,使用向上排空气法对气体进行收集;
故答案为:ACE;浓硫酸;
(2)过氧化氢溶液制取氧气的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;反应中的二氧化锰是反应的催化剂,在反应前后其质量和化学性质不变,仍可以继续使用;
故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;反应中的二氧化锰是反应的催化剂,在反应前后其质量和化学性质不变,仍可以继续使用;
(3)生成的氧气有少量溶解在水中,因此根据化学方程式计算获得的氧气理论值总是比实际实验操作收集到气体的数值大;
故答案为:生成的氧气有少量溶解在水中;
(4)根据反应的化学方程式为X+8H2O2=2CO2↑+N2↑+12H2O,生成物的2个CO2分子、1个N2分子和12个H2O分子中共含C、H、O、N原子的个数依次为2、24、16、2;而反应前的8个H2O2分子中只含有16个H原子和16个O原子;根据化学变化前后原子种类、数目不变,则偏二甲肼X的分子中含有2个C原子、8个H原子和2个N原子,其化学式可表示感谢为C2H8N2;
故答案为:C2H8N2;
(5)制取氨气是固体与固体反应,且需要加热制取气体,发生装置便可选择“固固加热型”的装置,氨气极易溶于水因此不能用排水集气法,密度比空气小所以可用向下排空气法收集气体,故选A,D;氨气溶于水显碱性,能使红石蕊试纸变蓝;
故答案为:A,D;变蓝.
点评 本题考查了利用过氧化氢制取氧气的操作及实验分析、利用化学方程式推断化学式等内容,难度较大.

 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案| A. | 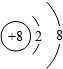 | B. | 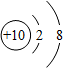 | C. | 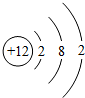 | D. | 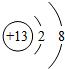 |
| A. | CO | B. | N2 | C. | NO2 | D. | NO |
| 农作物 | 棉花 | 玉米 | 大豆 | 茶树 |
| pH | 6.1-6.8 | 6.0-7.0 | 6.5-7.5 | 5.0-5.5 |
| A. | 棉花 | B. | 玉米 | C. | 大豆 | D. | 茶树 |
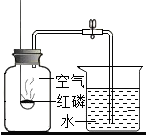 如图装置常用来测定空气中氧气的含量,下列对该实验的认识中正确的是( )
如图装置常用来测定空气中氧气的含量,下列对该实验的认识中正确的是( )| A. | 燃烧匙中的红磷可以换成细铁丝 | |
| B. | 红磷燃烧时就打开止水夹 | |
| C. | 红磷的量足会导致进入集气瓶中水的体积大于$\frac{1}{5}$ | |
| D. | 该实验可说明N2难溶于水 |
| A. | 二氧化硫----无色无味气体---化学式 SO2 | |
| B. | 氯化铁溶液------浅绿色-----溶质是FeCl2 | |
| C. | 两个氢氧根离子-----2OH- | |
| D. | 氧化镁中镁元素的化合价--------$\stackrel{2+}{Mg}$O |