题目内容
下列叙述中,正确的是( )
|
| A. | 酸和碱中都一定含有氢、氧两种元素 |
|
| B. | 能跟碱反应生成盐和水的化合物不一定是酸 |
|
| C. | 有盐参加的反应都是复分解反应 |
|
| D. | 生成盐和水的反应都是中和反应 |
| 氧化物、酸、碱和盐的概念;中和反应及其应用;复分解反应及其应用.. | |
| 专题: | 物质的分类;常见的酸 酸的通性. |
| 分析: | 根据已有的概念进行分析,酸是指电离时生成的阳离子全部是氢离子的化合物,碱是指电离时生成的阴离子全部是氢氧根离子的化合物,中和反应是指酸和碱的反应. |
| 解答: | 解:A、酸中一定含有氢元素,不一定含有氧元素,例如HCl,故A错误; B、能跟碱反应生成盐和水的化合物不一定是酸,例如二氧化碳能与氢氧化钠反应生成碳酸钠和水,故B正确; C、有盐参加的反应不一定是复分解反应,例如铁和硫酸铜溶液的反应时置换反应,故C错误; D、生成盐和水的反应不一定都是中和反应,例如金属氧化物和酸的反应,故D错误; 故选B. |
| 点评: | 本题考查了有关的概念,完成此题,可以依据概念进行.要求同学们熟练掌握有关的概念并理解,以便灵活应用. |

我国劳动人民早在五千年前就会使用木炭炼铜。在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙)。化学兴趣小组采用图乙装置,开展以下探究活动。

【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】(1)木炭与CuO的反应是:C + 2CuO  2Cu + CO2 ↑;若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O)。
2Cu + CO2 ↑;若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O)。
(2)Cu2O是红色固体,能与稀硫酸反应:Cu2O + H2SO4 = Cu + CuSO4 + H2O。
【作出猜想】红色固体的成分:①全部是Cu;②全部是Cu2O;③ ▲ 。
【实验探究】(1)取木炭、CuO两种黑色粉末适量,再与少许CaCl2(能降低反应温度、加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内。
(2)按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水 ▲ ,此时停止加热。
(3)待玻璃管冷却后,提取里面的红色固体,进行如下的验证:
| 步 骤 | 现 象 | 结 论 |
| ①取1.44 g红色固体装入试管, 滴入足量的 ▲ ,充分反应 | 红色固体部分减少, 溶液变为 ▲ 色 | 猜想 ▲ 错误 |
| ②滤出试管中残留的红色固体, 洗涤干燥,称其质量为1.04 g | 猜想 ▲ 正确 |
【评价反思】(1)使用图乙装置与使用图甲装置相比,其优点是 ▲ (写出1条即可)。
(2)若要证明CaCl2是该反应的催化剂,还需要验证CaCl2的 ▲ 。
(3)在铜的冶炼史中,我国劳动人民还有一项重大发明就是“湿法炼铜”。该方法可用化学方程式表示为 ▲ 。
植物因缺氮元素会引起叶片发黄,这时应该施加下列哪种肥料( )
|
| A. | NH4NO3 | B. | K2SO4 | C. | KCl | D. | Ca(H2PO4)2 |
有三瓶失去标签的无色溶液,已知它们分别是HCl溶液、BaCl2溶液、NaOH溶液中的一种.下列四种试剂中,能将上述三种无色溶液一次鉴别出来的是( )
|
| A. | CuSO4溶液 | B. | H2SO4溶液 | C. | MgCl2溶液 | D. | 酚酞试液 |


 的少量的C02并收集一瓶C0的装置如下图(瓶内为澄清石灰水), 其中最合理的装置是_ 。
的少量的C02并收集一瓶C0的装置如下图(瓶内为澄清石灰水), 其中最合理的装置是_ 。

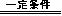 X十4H2O,
X十4H2O, 石油等矿物能源
石油等矿物能源