题目内容
8.用CO2和NH3合成尿素,是固定和利用CO2的成功范例,尿素的化学式为CO(NH2)2.其反应的化学方程式为:CO2+2NH3═CO(NH2)2+H2O.下列说法正确的是( )| A. | 尿素中有2个氮原子 | |
| B. | 尿素中碳、氧、氮、氢元素的质量比为3:4:7:1 | |
| C. | 参加反应的CO2与NH3的质量比是44:17 | |
| D. | 该反应是充分利用CO2的一种有效途径 |
分析 A、根据尿素的微观构成,进行分析判断.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据CO2+2NH3═CO(NH2)2+H2O,进行分析判断.
D、根据用CO2和NH3合成尿素,是固定和利用CO2的成功范例,进行分析判断.
解答 解:A、尿素是由尿素分子构成的,1个尿素分子中含有2个氮原子,故选项说法错误.
B、尿素中碳、氢、氮、氧元素的质量比为12:(1×2×2):(14×2):16=3:1:7:4,故选项说法正确.
C、由反应的化学方程式:CO2+2NH3═CO(NH2)2+H2O,参加反应的CO2与NH3的质量比是44:(17×2)=22:17,故选项说法错误.
D、用CO2和NH3合成尿素,是固定和利用CO2的成功范例,该反应是充分利用CO2的一种有效途径,故选项说法正确.
故选:BD.
点评 本题难度不大,理解题意,掌握化学式的有关计算、化学式的含义等是正确解答本题的关键.

练习册系列答案
相关题目
18.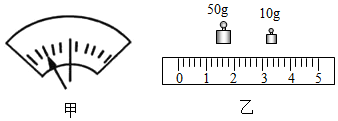 某同学用托盘天平称量药品,药品放在了左边,天平指针如甲图所示开始称量,称量完毕后示数如图乙所示,则实际称量药品的质量为( )
某同学用托盘天平称量药品,药品放在了左边,天平指针如甲图所示开始称量,称量完毕后示数如图乙所示,则实际称量药品的质量为( )
 某同学用托盘天平称量药品,药品放在了左边,天平指针如甲图所示开始称量,称量完毕后示数如图乙所示,则实际称量药品的质量为( )
某同学用托盘天平称量药品,药品放在了左边,天平指针如甲图所示开始称量,称量完毕后示数如图乙所示,则实际称量药品的质量为( )| A. | 大于62.4g | B. | 小于62.4g | C. | 大于57.6g | D. | 小于57.6g |
16.现甲、乙两化学小组安装两套如图1相同装置,通过测定产生相同体积气体所用时间长短来探究影响双氧水分解速率的因素.
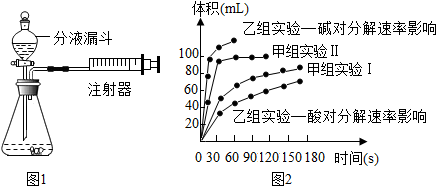
(1)下列方法能检查该装置气密性的是AB.
A.将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B.关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C.关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)甲小组有如下实验设计方案,完成下表.
(3)甲、乙两小组得出如图2数据.
甲组实验得出的数据可知:浓度越大,双氧水分解速率越快;
注意:若答对下面小题将奖励4分,但化学试卷总分不超过60分
(4)由乙组研究的酸、碱对双氧水分解影响因素的 数据分析:相同条件下,双氧水在碱(填“酸”或“碱”)性环境下放出气体速率较快.
(5)双氧水可以用过氧化钡固体与硫酸溶液反应制取,支持这一方案的理是过氧化氢在酸性环境下分解较慢.

(1)下列方法能检查该装置气密性的是AB.
A.将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B.关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C.关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)甲小组有如下实验设计方案,完成下表.
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究浓度对双氧水分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%双氧水 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%双氧水 |
甲组实验得出的数据可知:浓度越大,双氧水分解速率越快;
注意:若答对下面小题将奖励4分,但化学试卷总分不超过60分
(4)由乙组研究的酸、碱对双氧水分解影响因素的 数据分析:相同条件下,双氧水在碱(填“酸”或“碱”)性环境下放出气体速率较快.
(5)双氧水可以用过氧化钡固体与硫酸溶液反应制取,支持这一方案的理是过氧化氢在酸性环境下分解较慢.
3.我国科学家屠呦呦发现并提取了青蒿素,将其应用于医疗临床,首获诺贝尔自然科学 奖,青蒿素的化学式为C15H22O5,下列说法不正确的是( )
| A. | 该物质由 C、H、O 三种元素组成 | |
| B. | 该物质是氧化物 | |
| C. | 该物质的碳氢氧元素质量比为 90:11:40 | |
| D. | 该物质的一个分子,由 42 个原子构成 |
20.下列物质的用途中,利用其化学性质的是( )
| A. | 液氮用作冷冻剂 | B. | 氧气用于炼钢 | ||
| C. | 稀有气体做多种用途的电光源 | D. | 氢气用于填充探空气球 |
17.关于“物质-在氧气中燃烧的现象-所属反应类型”的描述中正确的是( )
| A. | 木炭-发出白光-化合反应 | |
| B. | 细铁丝-火星四射,生成红色固体-氧化反应 | |
| C. | 硫-微弱淡蓝色火焰-化合反应 | |
| D. | 石蜡-发出白光,瓶壁有水雾-化合反应 |
 2012年中国载人航天工程实现新突破,神舟九号航天员成功驾驶飞船与天宫一号目标飞行器对接.
2012年中国载人航天工程实现新突破,神舟九号航天员成功驾驶飞船与天宫一号目标飞行器对接. 某化学兴趣小组在做铁与硫酸铜溶液反应实验时,发现生成紫红色固体的同时还伴有少量气泡产生.为了进一步探究,他们又做了如下实验:
某化学兴趣小组在做铁与硫酸铜溶液反应实验时,发现生成紫红色固体的同时还伴有少量气泡产生.为了进一步探究,他们又做了如下实验: