题目内容
4.碳酸钙中钙元素的质量分数为多少?分析 根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:碳酸钙中钙元素的质量分数为:$\frac{40}{40+12+16×3}$×100%=40%
答:碳酸钙中钙元素的质量分数为40%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
12.下列有关说法正确的是( )
| A. | 摩尔是国际单位制中七个基本物理量之一 | |
| B. | 1mol H2约含6.02×1023个氢原子 | |
| C. | 1molSO2比1molSO3少1个氧原子 | |
| D. | 1 molCO和1 molCO2所含碳元素质量相等 |
9.某化学反应的微观示意图如图.下列说法正确的是( )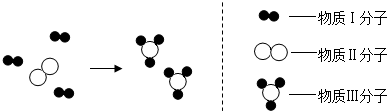

| A. | 该反应中原子种类、数目、质量不变,元素种类、质量、化合价不变 | |
| B. | 每3g物质Ⅰ与1g物质Ⅱ恰好完全反应生成2g物质Ⅲ | |
| C. | 该反应中反应物是单质,生成物一定是氧化物 | |
| D. | 该反应中每3n个物质Ⅰ分子与n个物质Ⅱ分子恰好完全反应生成2n个物质Ⅲ分子 |
16.下列现象的描述错误的( )
| A. | 木炭在氧气中燃烧发出白光 | |
| B. | 铁丝在氧气中燃烧剧烈火星四射 | |
| C. | 加热氯酸钾和二氧化锰的混合物生成使带火星木条复燃的无色气体 | |
| D. | 磷在氧气中燃烧生成白色烟雾 |

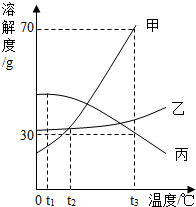 如图为甲、乙、丙三种固体物质溶解度曲线,据图回答:
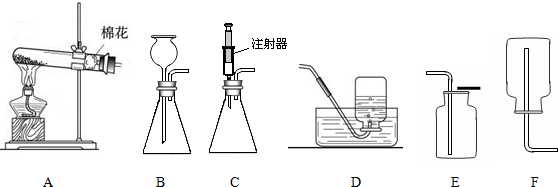
如图为甲、乙、丙三种固体物质溶解度曲线,据图回答: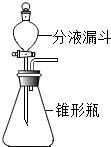 实验室用过氧化氢溶液在二氧化锰作催化剂的条伴下制取氧气.某学生设计了如图所示装置,可以通过分液漏斗的活塞控制液体的滴加速度.请回答下列问题:
实验室用过氧化氢溶液在二氧化锰作催化剂的条伴下制取氧气.某学生设计了如图所示装置,可以通过分液漏斗的活塞控制液体的滴加速度.请回答下列问题: