题目内容
19.氮氧化物(如N02、N0等)进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾.因此必须对含有氮氧化物的废气进行处理.(1)用氢氧化钠溶液可吸收废气中的氮氧化物.反应的化学方程式:N02+NO+2NaOH═2NaN02+H2O,产物NaN02中N元素的化合价为+3价;已知“HN02”读作“亚硝酸”,则NaN02的名称为亚硝酸钠.NaN02中氮、氧两种元素的质量比7:16
(2)氨气(NH3)也可用来处理氮氧化物.例如,氨气与二氧化氮反应:8NH3+6N02═7N2+12H2O.若某工厂排出废气中NO2含量为1.38%,则处理1.0×103米3这种废气,需要多少千克氨气(假设此时N02气体的密度为2.0克/升)?
分析 (1)首先要熟记常见元素(特别是不变价元素)与常见原子团的化合价以及化合价的规律原则,然后根据NaNO2中Na的化合价是+1价,O的化合价是-2价,利用化合价的原则(在化合物中正、负化合价的代数和为零)列方程解出NaNO2中N的化合价;
(2)利用体积分数公式及密度公式可求出二氧化氮的质量,而后利用8NH3+6NO2═7N2+12H20求出氨气的质量.
解答 解:(1)设NaNO2中N化合价是x.NaNO2中Na的化合价是+1价,O的化合价是-2价,利用化合物中各元素的化合价的代数和为零的原则得到方程
(+1)×1+x+(-2)×2=0
解得,x=+3
所以NaNO2中N的化合价是+3价.
故答案为:+3价;
已知“HNO2”读作“亚硝酸”,据盐化学式的读法,先读酸根再读金属元素;
故答案为:亚硝酸钠;
NaN02中氮、氧两种元素的质量比:14:(16×2)=7:16;
故填:7:16;
(1)+3 亚硝酸钠 7:16
(2)m=ρV=2.0克/分米3×1×106分米3×1.38%=27.6克
设氨气的质量为x
8NH3+6NO2=7N2+12H20
136 276
x 27.6g
$\frac{136}{276}=\frac{x}{27.6g}$
x=13.6kg
答:氨气的质量为13.6克.
点评 本题考查了常见元素与常见原子团的化合价以及化合价的规律,这类题几乎是在所有类型化学试题中都会出现.同时本题加强了和物理知识的整合,考察学生利用化学方程式计算的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列叙述不符合实验事实的是( )
| A. | 在Na2CO3、K2SO4、AgNO3三种溶液中分别滴入BaCl2溶液,都有白色沉淀生成 | |
| B. | 将氯化铵与氢氧化钠溶液混合加热后,会有刺激性气味的气体产生 | |
| C. | 未密封保存的苛性钠放在空气中质量会增加 | |
| D. | 将Cu(OH)2加入到滴有酚酞试液的蒸馏水中,溶液显红色 |
4.实验室一般不用块状石灰石与稀硫酸反应制取二氧化碳,原因是碳酸钙与硫酸反应生成的硫酸钙微溶,覆盖在石灰石的表面阻止与硫酸充分接触而终止反应.小明查阅资料后发现,在石灰石与硫酸反应停止后,加入少量氯化钠固体,能使反应继续进行,而加入少量的硝酸钾或硫酸铵固体却没现象.氯化钠中哪种成分促使石灰石与硫酸持续反应呢?小明设计了如下实验:向5支试管里各加入一块大小相近的石灰石和5毫升溶质质量分数为50%的硫酸,待反应停止后,再分别加入约0.2克的NaCI、KCl、NH4Cl、NaNO3、Na2SO4固体轻轻振荡.观察到的现象记录于表:
(1)实验中5支试管中反应有快慢,请你列举一种判断反应快慢的方法:比较相同时间内产生气泡的多少.
(2)小明为了研究Na+在实验中的作用,你认为应选择哪几组实验进行观察?1、2、3.
(3)通过实验可得出的结论是加快石灰石与硫酸反应是Na+与Cl-共同起作用;Cl-所起的用比Na+大.
| 实验组次 | 1 | 2 | 3 | 4 | 5 |
| 物质 | NaCl | KCl | NH4Cl | NaNO3 | Na2SO4 |
| 现象 | 继续发生反应生成气体,速度较快 | 继续反应生成气体,速度较慢 | 继续反应生成气体,速度较慢 | 没有很明显可见的现象 | 没有很明显可见的现象 |
(2)小明为了研究Na+在实验中的作用,你认为应选择哪几组实验进行观察?1、2、3.
(3)通过实验可得出的结论是加快石灰石与硫酸反应是Na+与Cl-共同起作用;Cl-所起的用比Na+大.
8.推理是学习化学的重要方法,下列推理正确的是( )
| A. | 分子可以构成物质,所以物质都是由分子构成 | |
| B. | 碱性溶液能使酚酞溶液变红色,则常温下能使酚酞溶液变红色的溶液的pH一定大于7 | |
| C. | 中和反应生成盐和水,所以生成盐和水的反应都是中和反应 | |
| D. | 单质是由同种元素组成,所以同种元素组成的物质都是纯净物 |
9.在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表,下列说法中不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 18 | 1 | 2 | 32 |
| 反应后质量/g | X(未知) | 26 | 2 | 12 |
| A. | 甲是生成物 | B. | 丙可能是该反应的催化剂 | ||
| C. | 反应中乙、丁的变化质量为13:6 | D. | 反应中甲、丁的变化质量为1:4 |
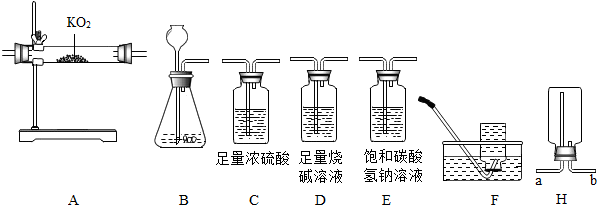

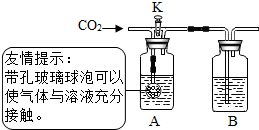 小刚和小丽两位同学用下图所示装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应.
小刚和小丽两位同学用下图所示装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应.