题目内容
5.通常用的食醋中含有3%-5%的乙酸(化学式C2H4O2),有关乙酸的说法正确的是( )| A. | 乙酸是一种氧化物 | |
| B. | 6g乙酸中含有2.4g碳元素 | |
| C. | 乙酸的相对分子质量为60g | |
| D. | 一个乙酸分子中含有2个碳原子、4个氢原子、1个氧分子 |
分析 A.根据氧化物的概念来分析;
B.根据化合物中所含元素的质量计算方法来分析;
C.根据相对分子质量的单位来分析;
D.根据分子结构来分析.
解答 解:A.氧化物中含有两种元素,而醋酸中含有碳、氢、氧三种元素,故错误;
B.6g乙酸中含有碳元素的质量=6g×$\frac{12×2}{12×2+1×4+16×2}×100%$=2.4g,故正确;
C.相对分子质量的单位不是“g”而是“1”,通常省略不写,故错误;
D.分子是由原子构成的,分子中不存在分子,故错误.
故选B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
7.下列说法正确的是( )
| A. | NaNO2是一种氧化物 | |
| B. | NaNO2是由三种元素组成 | |
| C. | NaNO2中氮元素的化合价为-3价 | |
| D. | NaNO2中Na、N、O三种元素的质量比为1:1:2 |
13.如图所示的实验操作不正确的是( )
| A. | 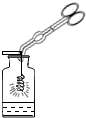 铁丝在氧气中燃烧 | B. |  读取液体的体积 | ||
| C. | 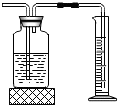 测定高锰酸钾分解生成氧气的体积 | D. | 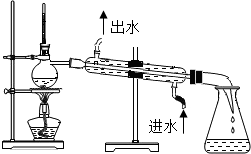 制取蒸馏水 |
10.分类是学习化学的方法之一,下列各组物质不是按单质、氧化物、混合物的顺序排列的是( )
| A. | 氢气、五氧化二磷、稀盐酸 | |
| B. | 液氮、生石灰、高锰酸钾完全分解后的剩余固体 | |
| C. | 氧气、冰水混合物、空气 | |
| D. | 稀有气体、氢氧化钙、石灰石 |
17.下列实验操作或数据中,正确的是( )
| A. | 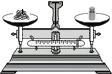 称量10.05g固体 | B. |  加热液体 | C. |  检查气密性 | D. | 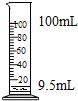 量取9.5mL液体 |
15.如图是几张微粒的结构示意图,有关说法错误的是( )
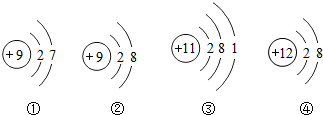

| A. | 微粒②和④核外电子排布相同,属于同种元素 | |
| B. | 微粒①易得到电子 | |
| C. | 微粒③易形成带一个单位正电荷的阳离子 | |
| D. | 微粒④带两个单位正电荷 |