题目内容
5.探究物质性质:
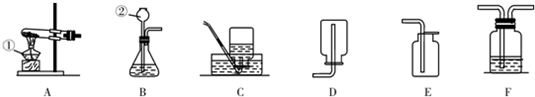
(1)图1二氧化碳是否可以溶于水,很难直接观察到现象,可以根据矿泉水瓶变瘪现象说明CO2能溶于水;
(2)图2研究氢氧化钠溶解于水时是吸热还是放热,是利用U型管内液面的变化引起了U形管内水位的变化,使b(填“a”或“b”)处的水位升高;
(3)图3观察气球胀大现象,说明CO2和NaOH发生了反应;
(4)图4产生气泡较快的金属是镁.
分析 (1)根据二氧化碳溶于水后,是塑料瓶内的压强减小进行分析;
(2)根据氢氧化钠溶于水,溶液温度试管,集气瓶内的压强增大进行分析;
(3)根据二氧化碳会与氢氧化钠反应进行分析;
(4)根据金属的活动性越强,与酸反应的速率越快进行分析.
解答 解:(1)二氧化碳溶于水后,是塑料瓶内的压强减小,所以可以根据矿泉水瓶变瘪现象说明CO2能溶于水;
(2)氢氧化钠溶于水,溶液温度试管,集气瓶内的压强增大,所以利用U型管内液面的变化引起了U形管内水位的变化,使b处的水位升高;
(3)二氧化碳会与氢氧化钠反应,所以图3观察气球胀大现象,说明CO2和NaOH发生了反应;
(4)金属的活动性越强,与酸反应的速率越快,所以图4产生气泡较快的金属是镁.
故答案为:(1)矿泉水瓶变瘪;
(2)U型管内液面,b;
(3)气球胀大现象;
(4)镁.
点评 本题考查了化学实验的操作以及有关的实验结论的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
20.首先通过实验证明空气中含有氧气和氮气的科学家是( )
| A. | 拉瓦锡 | B. | 门捷列夫 | C. | 阿伏伽德罗 | D. | 道尔顿 |
10.某厂年产纯碱120万吨,是我国三大纯碱生产企业之一.它的产品除了纯碱外,还有氧化钙和碳酸氢钠.该厂生产纯碱的工艺流程可简单表示如图
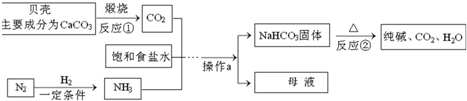
其生产过程中涉及到的主要化学反应有:
①NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓ ②2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O 请回答:
(1)反应①的化学方程式CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
(2)经过操作a析出晶体后的母液是的HCO3的饱和(填“饱和”或“不饱和”)溶液.写出母液中所有溶质的化学式:NaHCO3、NH4Cl、NaCl
(3)该厂母液中氯化铵(写名称)可作化肥中的氮肥,它也可与Ca(OH)2在加热时发生反应,写出该反应的化学方程式:Ca(OH)2+2NH4Cl=CaCl2+H2O+CO2↑.
(4)此流程中可以循环利用的物质是CO2(写化学式)

| 20摄氏度一些物质的溶解度(g) | |||
| 氯化钠 | 氯化铵 | 碳酸氢钠 | 碳酸氢铵 |
| 35.9 | 37.2 | 9.6 | 21.7 |
①NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓ ②2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O 请回答:
(1)反应①的化学方程式CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
(2)经过操作a析出晶体后的母液是的HCO3的饱和(填“饱和”或“不饱和”)溶液.写出母液中所有溶质的化学式:NaHCO3、NH4Cl、NaCl
(3)该厂母液中氯化铵(写名称)可作化肥中的氮肥,它也可与Ca(OH)2在加热时发生反应,写出该反应的化学方程式:Ca(OH)2+2NH4Cl=CaCl2+H2O+CO2↑.
(4)此流程中可以循环利用的物质是CO2(写化学式)
3.某密闭容器内有X、Y、Z、W四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:
下列说法正确的是C.
A.反应后X的质量为8g
B.Z与W的相对分子质量比一定是1:1
C.参加反应的X与Z的质量比是2:3
D.该反应属于置换或复分解反应(填反应类型)
| 物质 | X | Y | Z | W |
| 反应前质量/g | 4 | 1 | 10 | 2 |
| 反应后质量/g | 待测 | 5 | 4 | 8 |
A.反应后X的质量为8g
B.Z与W的相对分子质量比一定是1:1
C.参加反应的X与Z的质量比是2:3
D.该反应属于置换或复分解反应(填反应类型)