题目内容
14.一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量见表,下列税说法正确的是( )| 物质 | a | b | c | d |
| 反应前物质质量/g | 18 | 1 | 2 | 32 |
| 反应后物质质量/g | 待测 | 26 | 2 | 12 |
| A. | 待测数据是23 | B. | 参加反应a、d的质量比为4:1 | ||
| C. | 该反应的基本类型为化合反应 | D. | c物质一定是该反应的催化剂 |
分析 本题可分析b、c、d三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定a是反应物还是生成物,进而可以确定反应类型.
解答 解:由表中数据分析可知,反应前后b的质量增加了26g-1g=25g,故b是生成物,生成的b的质量为25g;同理可以确定d是反应物,反应的d的质量为32g-12g=20g;
由表中数据分析可知,c的质量不变,可能作该反应的催化剂,也可能没有参加反应;由质量守恒定律,a应是反应物,且参加反应的a的质量为25g-20g=5g,故待测的数值为18g-5g=13g.
A、由以上分析可知,待测数据是13,选故项说法错误.
B、参加反应a、d的质量比,5g:20g=1:4,选故项说法错误.
C、该反应的反应物为a和d,生成物是b,符合“多变一”的特征,属于化合反应,故选项说法正确.
D、c的质量不变,可能作该反应的催化剂,也可能没有参加反应,故选项说法错误.
故选C.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
2.用数轴表示某些化学知识直观、简明、易记.下列表示不正确的是( )
| A. | $→_{地壳中部分元素的含量}^{氧硅铝(小)}$ | |
| B. | $→_{硫元素的化合价}^{H_{2}S、S、SO_{2}、H_{2}SO_{4}(高)}$ | |
| C. | $→_{部分元素原子序数的关系}^{H、C、Na、Mg(大)}$ | |
| D. | $→_{粒子的体积关系}^{离子、原子、分子(大)}$ |
19.某石灰水中含有氢氧化钙1.48g,要使石灰水中含有氢氧化钙全部转化为碳酸钙沉淀,生成的沉淀质量是多少?标准状况下需要通入二氧化碳气体体积是多少升?(标准状况下二氧化碳气体的密度是1.96g/L)
6.下列关于化学反应的实验现象描述正确的是( )
| A. | 打开盛有浓盐酸的试剂瓶,看到瓶口有大量白雾 | |
| B. | 在电解水实验中,正负两极产生的气体体积比约为2:1 | |
| C. | 木炭在空气中燃烧生成黑色有刺激性气味的气体 | |
| D. | 铁丝在氧气中剧烈燃烧,火星四射,放出大量热,生成四氧化三铁 |
3.做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气等物质.
【实验验证】
【总结反思】丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸.兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气等物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变红色 | 猜想(3)成立 |
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
4.一定温度下,一定质量的氢氧化钠固体溶于水制成溶液.下列有关的量不随水的质量改变而改变的是( )
| A. | 溶液质量分数 | B. | 溶液的pH | ||
| C. | 氢氧化钠的溶解度 | D. | 最多能吸收二氧化碳的质量 |
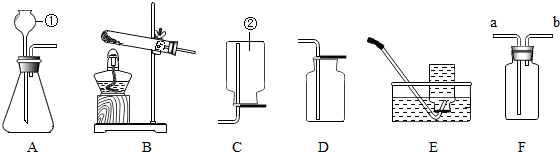
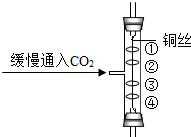 A(填字母),若选择F装置收集H2S,气体应该从a(填“a”或“b”)端进入,实验结束后剩余的H2S气体用氢氧化钠溶液吸收,吸收的目的是防止硫化氢污染空气.
A(填字母),若选择F装置收集H2S,气体应该从a(填“a”或“b”)端进入,实验结束后剩余的H2S气体用氢氧化钠溶液吸收,吸收的目的是防止硫化氢污染空气.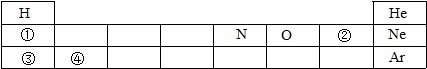
 .
.