题目内容
2.纯净的氢气在空气中燃烧,下列现象不符合事实的是( )| A. | 用冷而干燥的烧杯罩在火焰上方,烧杯内壁有水珠生成 | |
| B. | 接触烧杯感到发烫 | |
| C. | 产生淡蓝色火焰 | |
| D. | 氢分子和氧分子结合成水分子 |
分析 根据纯净的氢气在空气中燃烧的现象,进行分析判断即可.
解答 解:A、纯净的氢气在空气中燃烧,用冷而干燥的烧杯罩在火焰上方,烧杯内壁有水珠生成,故选项不符合题意.
B、纯净的氢气在空气中燃烧,放出大量的热,接触烧杯感到发烫,故选项不符合题意.
C、纯净的氢气在空气中燃烧,产生淡蓝色火焰,故选项不符合题意.
D、纯净的氢气在空气中燃烧,从微观上是因为氢分子分裂成了氢原子,氧分子分成了氧原子,然后氢原子、氧原子重新组合形成水分子,但是微观上观察不到,不属于实验现象,故选项符合题意.
故选:D.
点评 本题难度不大,掌握氢气在空气中燃烧的现象、实验现象与实验结论等的区别是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.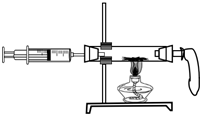 如图为测定空气中氧气的体积分数的实验装置.
如图为测定空气中氧气的体积分数的实验装置.
(1)实验前,连接好装置,把注射器活塞向里推,使气球鼓起,然后保持活塞不动.隔一会儿,观察到气球不变瘪(填“不变瘪”、“变瘪”),则装置气密性良好.
(2)加热过程中,可观察到的现象是红色的铜粉逐渐变为黑色.发生的反应文字表达式或化学方程式为:铜+氧气$\stackrel{加热}{→}$氧化铜,或2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
(3)实验过程中,记录的数据如下:
由表中数据可知实验中消耗的氧气的体积为20ml.
由此可以初步得出:空气中氧气约占总体积的五分之一.
(4)(单选)若实验测得空气中氧气的含量偏高,可能的原因是D(填序号).
A.实验前,注射器内空气的体积大于装置内空气总体积的1/5
B.使用的铜粉的量不足
C.加热时反复推拉注射器活塞
D.反应结束,待装置冷却到室温后,测注射器内剩余气体体积时,气球内残留有气体.
 如图为测定空气中氧气的体积分数的实验装置.
如图为测定空气中氧气的体积分数的实验装置.(1)实验前,连接好装置,把注射器活塞向里推,使气球鼓起,然后保持活塞不动.隔一会儿,观察到气球不变瘪(填“不变瘪”、“变瘪”),则装置气密性良好.
(2)加热过程中,可观察到的现象是红色的铜粉逐渐变为黑色.发生的反应文字表达式或化学方程式为:铜+氧气$\stackrel{加热}{→}$氧化铜,或2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
(3)实验过程中,记录的数据如下:
| 实验前注射器内气体的体积/ml | 硬质玻璃管的容积/ml | 试验后注射器内剩余的气体体积/ml | 消耗的氧气体积/ml |
| 30 | 70 | 10 |
由此可以初步得出:空气中氧气约占总体积的五分之一.
(4)(单选)若实验测得空气中氧气的含量偏高,可能的原因是D(填序号).
A.实验前,注射器内空气的体积大于装置内空气总体积的1/5
B.使用的铜粉的量不足
C.加热时反复推拉注射器活塞
D.反应结束,待装置冷却到室温后,测注射器内剩余气体体积时,气球内残留有气体.
11.如图是元素周期表中硅元素的图例说明,下列有关图例的说法不正确的是( )
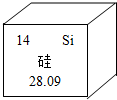

| A. | “Si”表示硅的元素符号 | |
| B. | “14”指的是硅元素的原子序数 | |
| C. | “硅”是元素名称,硅属于非金属元素 | |
| D. | “28.09”指一个硅原子的质量是基准碳原子质量的28.09倍 |

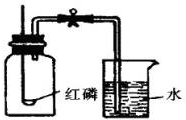 按如图组装仪器,关闭弹簧夹,红磷燃烧.请回答下列问题:
按如图组装仪器,关闭弹簧夹,红磷燃烧.请回答下列问题: