题目内容
14.铁是人类广泛使用的金属,回答有关问题:(1)工业上用赤铁矿石炼铁的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)为了防止铁制品生锈,经常在铁制品表面刷“银粉”,其防锈原理是隔绝氧气和水.
(3)稀盐酸除铁锈的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O.
分析 工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳;金属与水、氧气充分接触时容易生锈,使金属制品与氧气和水隔绝可以防止生锈;铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,写出反应的化学方程式即可.
解答 解:(1)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)为了防止金属的锈蚀,人们常采用在其表面刷漆、涂油或镀上其他金属等覆盖保护膜的方法,这些方法都能够防止锈蚀的共同原理是隔绝氧气和水.
(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.
答案:(1)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)隔绝氧气和水;(3)Fe2O3+6HCl═2FeCl3+3H2O.
点评 本题难度不大,掌握工业上炼铁的反应原理、防止金属生锈的措施等是正确解答本题的关键.

练习册系列答案
相关题目
5.将金属锰(Mn)投入稀盐酸中,有气泡产生.将铝条插入氯化锰溶液中,如果有锰析出,则Mn、Al、Ag的金属活泼性由强到弱的顺序是( )
| A. | Mn、Al、Ag | B. | Al、Mn、Ag | C. | Ag、Al、Mn | D. | Ag、Mn、Al |
6.月球的土壤中吸附着数百万吨的氦(He-3),其原子核中质子数为2,中子数为1,下列关于 He-3的说法正确的是( )
| A. | 原子核外电子数为3 | B. | 相对原子质量为2 | ||
| C. | 原子的核电荷数为3 | D. | 原子结构示意图为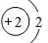 |
3.分类、类比是学习化学常用的有效方法.请回答:
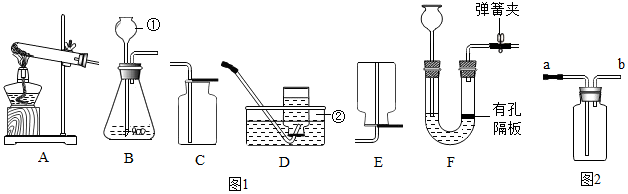
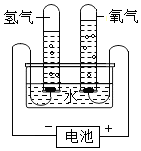
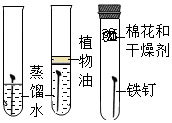
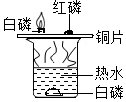
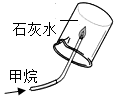
(1)初中化学教材中有很多实验,若按照实验目的不同来分类,可以将下表中的②③;①④(填字母)归为一类,依据是:②③都是探究反应发生的条件;①④都是探究物质的性质.
(2)在金属活动性顺序中,钙的活动性较强,不-能与活动性位于它之后的金属的盐溶液直接发生置换反应,而是先和水发生反应.已知金属钙和水反应的化学方程式为:Ca+2H2O═Ca(OH)2+H2↑.则将金属钙投入氯化铵溶液中会观察到的现象是:溶液中有气泡产生,并产生刺激性气味.试写出该过程的总反应的化学方程式Ca+2NH4Cl═CaCl2+H2↑+2NH3↑.
(1)初中化学教材中有很多实验,若按照实验目的不同来分类,可以将下表中的②③;①④(填字母)归为一类,依据是:②③都是探究反应发生的条件;①④都是探究物质的性质.
 |  |  |  |
| ① | ② | ③ | ④ |
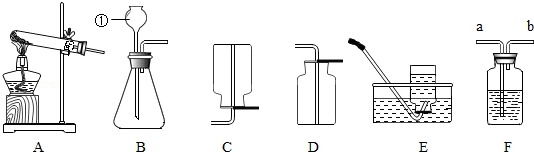
 在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙还有剩余固体,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙中固体析出,丙固体没有明显变化.
在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙还有剩余固体,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙中固体析出,丙固体没有明显变化.