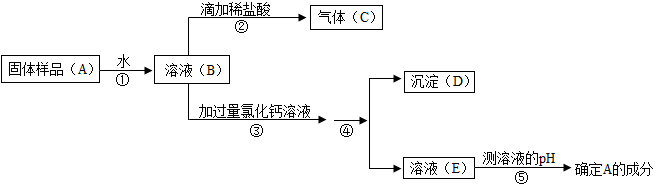
题目内容
16.小明在社会实践中喜欢收集各种颜色的矿石.他收集到下列矿石样品.
(1)上述矿石的主要成分为氧化物的是A.
(2)赤铁矿可用来炼铁,工业上用赤铁矿炼铁的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.用含氧化铁50%的赤铁矿500吨炼铁,理论上炼出铁的质量为500t×50%×$\frac{112}{160}×100%$(写计算式).
分析 (1)根据矿石主要成分的组成以及氧化物的概念分析判断;
(2)根据赤铁矿的主要成分是氧化铁,工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,写出反应的化学方程式并根据化学式进行计算即可.
解答 解:(1)赤铁矿的主要成分是Fe2O3,是由两种元素组成的且有一种是氧元素的化合物,属于氧化物;孔雀石中主要成分是Cu2(OH)2CO3是由四种元素组成的化合物,不属于氧化物;闪锌矿的主要成分是ZnS,是不含氧元素的化合物,不属于氧化物;黄铁矿的主要成分是FeS2,不含有氧元素,不属于氧化物;故填:A;
(2)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
由质量守恒定律可知,反应前后铁元素的质量不变,则理论上可炼出铁的质量为:500t×50%×$\frac{112}{160}×100%$=175t;故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;500t×50%×$\frac{112}{160}×100%$.
点评 本题所考查的金属的知识点较多,但难度不大,应加强金属知识的归纳和学习.

练习册系列答案
相关题目
10.“推理”是化学学习过程中常用的思维方法.现有以下推理,其中正确的是( )
| A. | 因为碱的溶液呈碱性,所以呈碱性的溶液一定是碱的溶液 | |
| B. | 单质中只含有一种元素,所以只含有一种元素的物质一定是单质 | |
| C. | 铁在潮湿的空气中会生锈,所以防止铁生锈要同时隔绝水和氧气 | |
| D. | 因为蜡烛燃烧生成二氧化碳和水,所以蜡烛组成里一定含有碳元素和氢元素 |
1.下列四个图象分别对应四个变化过程的一种趋势,其说法正确的是( )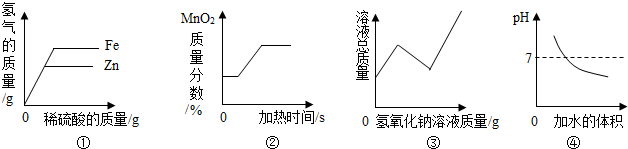
?①表示在等质量的铁粉和锌粉中分别加入足量的溶质质量分数相等的稀硫酸
?②用加热一定质量的氯酸钾和二氧化锰固体混合物的方法制取氧气
?③向一定量的硫酸和硫酸铜的混合溶液中逐滴加入10%的氢氧化钠溶液
④向一定量的氢氧化钠溶液中加水稀释,溶液的pH变化.

?①表示在等质量的铁粉和锌粉中分别加入足量的溶质质量分数相等的稀硫酸
?②用加热一定质量的氯酸钾和二氧化锰固体混合物的方法制取氧气
?③向一定量的硫酸和硫酸铜的混合溶液中逐滴加入10%的氢氧化钠溶液
④向一定量的氢氧化钠溶液中加水稀释,溶液的pH变化.
| A. | 上述图象只有2个正确 | |
| B. | 上述图象只有3个正确 | |
| C. | 上述图象全部正确 | |
| D. | 若将②?中的纵坐标改为固体总质量,该图象也能正确反映相应的变化趋势 |
2.C919所使用的下列材料,属于有机合成材料的是( )
| A. |  涤纶座套 | B. |  橡胶轮胎 | C. |  合金机身 |