题目内容
10.下列是初中化学部分重要的实验或实验装置,请按要求填空: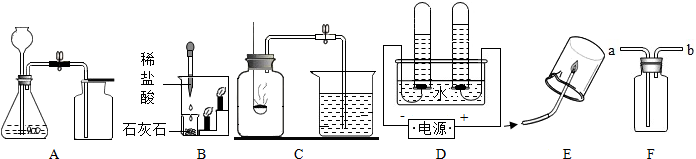
(1)写出用A装置制取一种气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑(或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑);
(2)B实验说明二氧化碳具有不能燃烧,不支持燃烧,密度比空气大的性质;
(3)C、D、E都是研究物质组成的实验.C实验是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的;D实验是水电解实验,通过证明生成物的元素种类来推断水的组成.E实验是通过燃烧甲烷,检验甲烷成分的实验.从研究方法分析,你认为E实验与D(选填“C”或“D”)实验的方法相同.
(4)如何用F装置收集一瓶较纯净的氧气?先用水将B装置灌满,然后将氧气从b端通入.
分析 (1)根据A装置的特点写化学方程式;
(2)根据蜡烛熄灭的顺序解答;
(3)通过测定空气里氧气含量的实验、电解水实验、甲烷燃烧实验的原理可以得出本题的答案.
(4)得到较为纯净的氧气可需用排水法.
解答 (1)A装置是固液常温型,所以可用来制取二氧化碳和氧气,化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑(或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑);
(2)B实验中下层的蜡烛先灭,上层的后灭,说明二氧化碳具有不能燃烧,不支持燃烧,密度比空气大;
(3)C实验是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的.D实验是通过证明生成物的组成元素来推断水的组成的.而C实验与D实验的方法相同;
(4)为得到较为纯净的氧气,用F装置收集可以用排水法,氧气应从导管b进,水从导管a排出.
故答案为:
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑(或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑)
(2)不能燃烧,不支持燃烧,密度比空气大
(3)D
(4)先用水将B装置灌满,然后将氧气从b端通入 (用排空气法不给分,不说从b端通入不给分)
点评 熟练掌握实验室中制取气体的发生装置和收集装置的选择依据,并能作出正确的选择,记住常见气体制取的反应原理,并能够正确书写化学方程式.

练习册系列答案
相关题目
20.小洁和小星两位同学,共同做了水的电解实验,并验证了两极的气体,有下列对话,其中正确的是( )
| A. | 小洁说:“正极产生的气体体积比负极多” | |
| B. | 小星说:“负极产生的气体体积比正极多” | |
| C. | 小洁说:“正极产生的气体能够被点燃” | |
| D. | 小星说:“负极上的气体能使带火星的木条复燃” |
18.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物.它的直径还不到人的头发丝粗细的$\frac{1}{20}$.虽然PM2.5只是地球大气成分中含量很少的组分,但它对空气质量和能见度等有重要的影响.像钢铁冶炼厂等会产生大量的可吸入颗粒物,某社会实践活动小组对某钢铁厂进行了参观,有一同学对工厂中的铁矿石样品和钢样进行实验、分析、计算,了解了该钢铁厂生产原料、产品的相关信息.下面请你根据他们的实验计算回答:
取该厂的某钢样粉末28.36g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到3g白色沉淀.
(1)计算此钢样粉末中铁和碳的质量之比.
(2)再取三份不同质量的钢样粉末分别加到50g质量分数相同的稀硫酸中,充分反应后,测得的实验数据如下表所示:
请根据表中数据计算稀硫酸中H2SO4的质量分数.
取该厂的某钢样粉末28.36g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到3g白色沉淀.
(1)计算此钢样粉末中铁和碳的质量之比.
(2)再取三份不同质量的钢样粉末分别加到50g质量分数相同的稀硫酸中,充分反应后,测得的实验数据如下表所示:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.836 | 5.672 | 8.508 |
| 生成气体的质量/g | 0.1 | 0.2 | 0.25 |
5.在化学的学习中,同学们知道:聚乙烯塑料只含C、H两种元素,如用焚烧方法处理废弃塑料会造成大气污染.化学兴趣小组对聚乙烯塑料在空气中燃烧生成的碳的氧化物组成进行探究.
提出猜想】A.只有CO2 B.只有CO C.既有CO2也有CO
【资料】微量CO遇到浸有磷钼酸溶液的氯化钯黄色试纸,立即变蓝;而CO2遇该试纸不变色
【方案】化学兴趣小组在老师的指导下,设计如图所示实验,通过观察装置B、装置C的实验现象,验证猜想.

【实验探究】请你帮助他们写成实验报告.
【讨 论】
(1)根据实验结论,从环保角度考虑,实验中应对尾气进行处理.处理方法是将尾气收集到气囊中(或将尾气点燃).
(2)聚乙烯塑料在空气中燃烧,生成物中除了CO2、CO外,还应有的物质是水.
提出猜想】A.只有CO2 B.只有CO C.既有CO2也有CO
【资料】微量CO遇到浸有磷钼酸溶液的氯化钯黄色试纸,立即变蓝;而CO2遇该试纸不变色
【方案】化学兴趣小组在老师的指导下,设计如图所示实验,通过观察装置B、装置C的实验现象,验证猜想.

【实验探究】请你帮助他们写成实验报告.
| 实验步骤 | 实验现象 | 实验结论及化学方程式 |
| 点燃酒精灯加热,随即打开弹簧夹,通入干燥的空气. 观察装置B、装置C中的现象 | 装置B中的现象是: 黄色试纸变蓝 装置C中的现象是: 澄清石灰水变浑浊 | 聚乙烯塑料在空气中燃烧,生成碳的氧化物中,既有CO2,也有CO. 装置C中反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O |
(1)根据实验结论,从环保角度考虑,实验中应对尾气进行处理.处理方法是将尾气收集到气囊中(或将尾气点燃).
(2)聚乙烯塑料在空气中燃烧,生成物中除了CO2、CO外,还应有的物质是水.
15.日常生活中,切开的苹果很快就会
“生锈”.小亮查到了相关资料:当苹果被切开时,
进入的氧气就会与苹果中的一些物质发生反应,使之变成褐色.苹果“生锈”以后,所含的维生素C会减少,影响营养价值.小亮对此展开探究:
猜想:苹果“生锈”可能与空气中的氧气有关.“生锈”的快慢还可能与温度有关.
实验:
(1)由甲与乙两组实验可以验证苹果“生锈”是否与空气中的氧气有关;
(2)实验结论之一:苹果“生锈”的速度与温度有关,温度越高,变色越快.请你补充乙组的实验结果:果肉表面“生锈”;
(3)为了防止切开后的苹果“生锈”,可以采取的措施有密封保存.
“生锈”.小亮查到了相关资料:当苹果被切开时,
进入的氧气就会与苹果中的一些物质发生反应,使之变成褐色.苹果“生锈”以后,所含的维生素C会减少,影响营养价值.小亮对此展开探究:
猜想:苹果“生锈”可能与空气中的氧气有关.“生锈”的快慢还可能与温度有关.
实验:
| 实验操作(观察30分钟) | 实验结果 | |
| 甲 | 将一小块苹果浸入装满蒸馏水(已除去氧气)的集气瓶中,观察现象. | 果肉表面不变色 |
| 乙 | 将一小块苹果放入充满氧气的集气瓶中,观察现象. | 果肉表面“生锈” |
| 丙 | 将一小块苹果放入充满氧气的集气瓶中,再浸入热水里,观察现象. | 果肉表面很快变色,颜色很深 |
(2)实验结论之一:苹果“生锈”的速度与温度有关,温度越高,变色越快.请你补充乙组的实验结果:果肉表面“生锈”;
(3)为了防止切开后的苹果“生锈”,可以采取的措施有密封保存.
2.下列有关溶液的说法中,正确的是( )
| A. | 饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 | |
| B. | 饱和溶液析出晶体后,就变成了不饱和溶液 | |
| C. | 无色的液体一定是溶液 | |
| D. | 饱和溶液和不饱和溶液在一定条件下可以互相转化 |