题目内容
12. 如图为某钙片的商品标签,请根据标签的有关信息完成下列各题:
如图为某钙片的商品标签,请根据标签的有关信息完成下列各题:(1)主要成分碳酸钙(CaCO3)中钙元素的质量分数(Ca%)=$\frac{40}{40+12+16×3}$×100%=40%(书写解题步骤).
(2)某儿童按标签用量服药,每天补充钙元素质量是2g×75%×40%=0.6g(书写解题步骤).
分析 根据碳酸钙的化学式,判断计算碳酸钙中钙元素的质量分数;根据标签中的成分可知钙片中碳酸钙的质量,利用钙元素在碳酸钙中的质量分数来计算.
解答 解:(1)碳酸钙中钙元素的质量分数是:$\frac{40}{40+12+16×3}$×100%=40%;
(2)某儿童按标签用量服药,每天补充钙元素质量是:2g×75%×40%=0.6g.
故答为:(1)$\frac{40}{40+12+16×3}$×100%=40%;(2)2g×75%×40%=0.6g.
点评 本题考查学生利用标签中的信息来分析解决问题,较好的训练学生抽取信息、利用信息,并结合所学知识来解答问题的能力.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
1.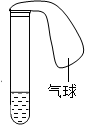 如图所示:试管中盛有某种液体,将气球中的某种固体小心地倒入试管中.下列各组物质中,不能使气球逐渐变大的是( )
如图所示:试管中盛有某种液体,将气球中的某种固体小心地倒入试管中.下列各组物质中,不能使气球逐渐变大的是( )
 如图所示:试管中盛有某种液体,将气球中的某种固体小心地倒入试管中.下列各组物质中,不能使气球逐渐变大的是( )
如图所示:试管中盛有某种液体,将气球中的某种固体小心地倒入试管中.下列各组物质中,不能使气球逐渐变大的是( )| A. | 铁粉和稀硫酸 | B. | 氯化钠和水 | C. | 镁和稀硫酸 | D. | 石灰石和稀盐酸 |
20.某种瘦肉精的化学式为C12H18OCl2N2.下列关于这种瘦肉精的说法正确的是( )
| A. | 是无机化合物 | |
| B. | 碳、氢、氧 3种元素的质量比为72:9:8 | |
| C. | 相对分子质量为277g | |
| D. | 由C12H18O、Cl2、N2 3种分子组成 |
1.在一定质量、一定质量分数的稀硫酸中,加入相同质量、相同质量分数的氢氧化钠溶液,则反应后溶液的pH应当是( )
| A. | 等于7 | B. | 小于7 | C. | 大于7 | D. | 无法确定 |
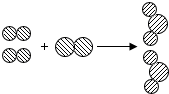 如图所示,
如图所示,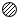 表示氢原子,
表示氢原子, 表示氧原子.试从物质组成、分子构成、物质变化的角度各说明一种观点.
表示氧原子.试从物质组成、分子构成、物质变化的角度各说明一种观点.