题目内容
6.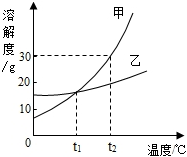 如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )| A. | 甲物质溶解度受温度影响比乙小 | |
| B. | t2℃时甲的饱和溶液的溶质质量分数小于30% | |
| C. | t1℃时,甲、乙饱和溶液的溶质质量分数相等 | |
| D. | 可采用降低温度的方法使乙的饱和溶液变为不饱和溶液 |
分析 根据固体物质的溶解度曲线可以:①某物质在某温度下的溶解度,②判断物质的溶解度随温度变化的变化情况,③比较不同物质在同一温度下的溶解度的大小;注意在同温度下的饱和溶液中溶质的质量分数和溶解度间的关系:$\frac{溶解度}{100g+溶解度}$×100%.
解答 解:A、比较甲、乙两物质的溶解度曲线可以看出,甲的溶解度曲线陡,乙的溶解度曲线缓,说明甲物质的溶解度受温度影响比乙物质的大,A错误;
B、t2℃时,甲的溶解度为30g,饱和溶液的溶质质量分数=$\frac{30g}{100g+30g}$×100%<30%,B错误;
C、t1℃时,甲、乙饱和溶液的溶解度相等,故甲、乙饱和溶液的溶质质量分数相等相等,故C正确;
D、乙的溶解度随温度的升高而升高,所以可以通过升高温度法使乙的饱和溶液变为不饱和溶液,故D错误.
故C正确.
点评 本题难度不大,主要考查了溶解度曲线的意义和溶质质量分数的应用.

练习册系列答案
相关题目
8.除去下列各物质中的少量杂质,所选用的试剂,方法不正确的是( )
| 选项 | 物质 | 杂质(少量) | 加入试剂及用量 |
| A | CO2 | CO | 通过灼热的氧化铜 |
| B | 铜粉 | 铁粉 | 足量的稀硫酸,过滤 |
| C | FeSO4溶液 | CuSO4溶液 | 加入足量的铁粉,过滤 |
| D | CO | CO2 | 通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
5.下列不属于氧气用途的是( )
| A. | 急救病人 | B. | 作燃料 | C. | 金属焊接 | D. | 动植物呼吸 |
11.氧是地壳中含量最多的元素,有两种氧原子可以分别表示为为${\;}_{8}^{16}$O和${\;}_{8}^{18}$O右下角数字表示质子数,右上角数字为质子数和中子数之和,则( )
| A. | ${\;}_{8}^{16}$O和${\;}_{8}^{18}$O互为同位素 | |
| B. | ${\;}_{8}^{16}$O的核外电子数多于${\;}_{8}^{18}$O | |
| C. | ${\;}_{8}^{16}$O和${\;}_{8}^{18}$O属于同种原子 | |
| D. | ${\;}_{8}^{16}$O和${\;}_{8}^{18}$O的核内中子数相等 |
18.下列物质的名称、俗名与化学式完全对应的是( )
| A. | 氯化钠 食盐 NaCl2 | B. | 碳酸氢钠 苏打 NaHCO3 | ||
| C. | 氢氧化钙 熟石灰 CaO | D. | 氢氧化钠 火碱 NaOH |
16.酸、碱、盐溶解性表是学习化学的重要工具.下表列出了部分酸、碱、盐在20℃时的溶解性.利用此表完成下列各小题:
(1)查:CaSO4的溶解性微溶;
(2)写出表中空格处物质的化学式H2O;
(3)运用此表,写出一个生成蓝色溶液且属于中和反应的化学方程式:Cu(OH)2+H2SO4═CuSO4+2H2O.
| 离子 | OH- | Cl- | SO42- |
| H+ | 溶、挥 | 溶 | |
| Na+ | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 微 |
| Cu2+ | 不 | 溶 | 溶 |
(2)写出表中空格处物质的化学式H2O;
(3)运用此表,写出一个生成蓝色溶液且属于中和反应的化学方程式:Cu(OH)2+H2SO4═CuSO4+2H2O.