题目内容
8.含氨15%的氨水2千克,稀释到含氨0.3%时,需要加水( )| A. | 98千克 | B. | 100千克 | C. | 102千克 | D. | 104千克 |
分析 根据溶液稀释前后溶质的质量不变,结合题意进行分析解答.
解答 解:设要加水的质量为x,根据溶液稀释前后溶质的质量不变,
则2kg×15%=(2kg+x)×0.3% x=98kg.
故选:A.
点评 本题难度不大,考查溶液的稀释问题,掌握溶液稀释前后溶质的质量不变是正确解答此类题的关键所在.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案
相关题目
19.水稻出现倒伏现象可能缺少以下哪种化肥( )
| A. | NH4NO3 | B. | K2CO3 | C. | Ca3(PO4)2 | D. | NH4HCO3 |
16.化学小组的同学探究二氧化碳与氢氧化钠的反应,实验方案如下:
(1)步骤①中气体鼓起的原因可能是NaOH溶液吸收CO2装置内压强变小,气球鼓起.
(2)步骤②中的操作是向外拉注射器3 (或充分振荡),其目的是证明步骤1中装置内的CO2已被完全吸收.
(3)步骤④中发生反应的化学方程式为Ca(OH)2+CO2═H2O+CaCO3↓.
(4)本实验的结论是CO2能和NaOH反应.
| 实验装置 | 实验步骤及操作 | 实验现象 |
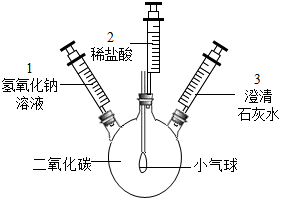 | ①将注射器1中的溶液推入充有CO2的瓶中 | 气球鼓起 |
| ②… | 无明显现象 | |
| ③将注射器2中的溶液推入瓶中 | 溶液中有气泡产生气球变瘪 | |
| ④向外拉注射器3 | 澄清石灰水变浑浊 |
(2)步骤②中的操作是向外拉注射器3 (或充分振荡),其目的是证明步骤1中装置内的CO2已被完全吸收.
(3)步骤④中发生反应的化学方程式为Ca(OH)2+CO2═H2O+CaCO3↓.
(4)本实验的结论是CO2能和NaOH反应.
12. 某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分.
某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分.
【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是
猜想一:CaO 猜想二:Ca(OH)2 猜想三:CaCO3 猜想四:Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是氧化钙能与水反应
【实验与事实】
【原理与呈现】请用化学方程式表示实验二中有关反应的化学反应原理:CaCO3+2HCl═CaCl2+CO2↑+H2O;Ca(OH)2+CO2═CaCO3↓+H2O.
【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用肥皂水来检测饮用水是硬水还是软水.
 某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分.
某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分.【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是
猜想一:CaO 猜想二:Ca(OH)2 猜想三:CaCO3 猜想四:Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是氧化钙能与水反应
【实验与事实】
| 实验 | 现象 | 结论 | |
| 实验一 | 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | 说明水垢中一定没有 氢氧化钙 |
| 实验二 | 按如图所示方案进行实验 | 反应一段时间后水垢消失,溶液澄清;玻璃片上澄清石灰水变浑浊 | 水垢中一定含有 碳酸钙 |
【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用肥皂水来检测饮用水是硬水还是软水.
9.鉴别如表各组物质的方法不正确的是( )
| 选项 | 鉴别的物质 | 鉴别的方法 |
| A | 纯水和矿泉水 | 观察是否澄清 |
| B | 硬水和软水 | 加肥皂水,振荡,观察泡沫的多少 |
| C | 水和过氧化氢溶液 | 加二氧化锰,观察是否有气泡 |
| D | 二氧化碳和氮气 | 加澄清石灰水,振荡,观察是否变浑浊 |
| A. | A | B. | B | C. | C | D. | D |
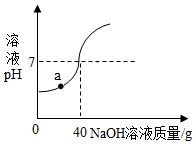 中和反应在工农业生产中应用广泛.现将溶质质量分数为10%的氢氧化钠溶液滴加到60g稀硫酸中,测得溶液pH与加入的氢氧化钠溶液的质量关系如图所示.
中和反应在工农业生产中应用广泛.现将溶质质量分数为10%的氢氧化钠溶液滴加到60g稀硫酸中,测得溶液pH与加入的氢氧化钠溶液的质量关系如图所示.