题目内容
8.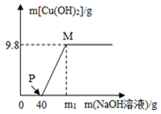 含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,则下列说法不正确的是( )
含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,则下列说法不正确的是( )| A. | m1的数值为80 | |
| B. | P点溶液中的溶质是氯化钠和氯化铜 | |
| C. | M点溶液中的溶质是氯化钠 | |
| D. | 整个反应过程中,溶液中氯离子个数不变 |
分析 由图中信息可知,氢氧化钠先和盐酸反应,当盐酸完全反应后,再和氯化铜反应,根据提供的数据可以求出相关方面的量.
解答 解:A、由图中可知,盐酸消耗的氢氧化钠溶液的质量是40g,氢氧化钠的质量是:40g×10%=4g,
生成氢氧化铜的质量是9.8g,
设氯化铜消耗的氢氧化钠的质量为x,
2NaOH+CuCl2═Cu(OH)2↓+2NaCl
80 98
x 9.8g
$\frac{80}{x}=\frac{98}{9.8g}$
x=3.65g,
氯化铜消耗的氢氧化钠溶液的质量为:$\frac{8.0g}{10%}$=80g,则沉淀完全时,消耗氢氧化钠溶液的质量是:40g+80g=120g,m1的数值为120.故不正确.
B、P点表示氢氧化钠与盐酸恰好反应,溶液中的溶质有:盐酸和氢氧化钠反应生成的氯化钠,还有没有反应的氯化铜,故正确.
C、M点表示氢氧化钠与盐酸、氯化铜都恰好反应,溶液中的溶质是盐酸和氢氧化钠反应生成的氯化钠,还有氢氧化钠与氯化铜反应生成的氯化钠,所以溶质只有氯化钠,故正确;
D、整个反应过程中,盐酸中的氯离子、氯化钠中的氯离子、氯化铜中的氯离子都是以离子形式存在,所以整个反应过程中,氯离子个数不变.故正确.
故选:A.
点评 根据化学方程式计算时,化学方程式要书写正确,特别是要配平,如果不配平,计算的结果就不规范,这是要注意的问题.

练习册系列答案
相关题目
3.青蒿素(分子式为C15H22O5),又名黄蒿素等,是从植物黄花蒿茎叶中提取的有过氧基团的倍半萜内酯药物,主要用于治疗多种恶性疟疾.2015年10月5曰,我国女药学家屠呦呦因发现了青蒿素而获得了 2015年诺贝尔生理学或医学奖.下列有关说法不正确的是( )
| A. | 青蒿素是一种有机物 | |
| B. | 在一个青蒿素分子中,C、H、O三种元素的原子个数比是15:22:5 | |
| C. | 青蒿素不属于氧化物 | |
| D. | 青蒿素分子中氧元素的化合价为-2价,则在生成该分子时,氧元素失去了两个电子 |
13.2014年4月兰州发生了自来水苯超标事故,已知苯的化学式为C6H6,下列有关说法正确的是( )
| A. | 苯中的C、H元素的质量比为12:1 | |
| B. | 苯是由6个碳元素和6个氢元素组成 | |
| C. | 苯分子中碳的原子结构示意图为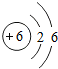 | |
| D. | 苯中碳、氢元素均位于元素周期表的第二周期 |
20.如图所示的实验操作中不正确的是( )
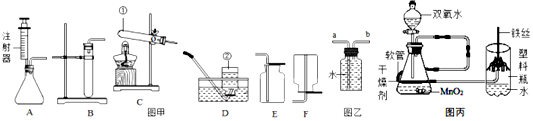
| A. | 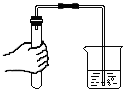 检查气密性 | B. |  加入固体药品 | C. |  滴加液体 | D. |  过滤粗盐水 |
17.某同学为了探究酸和碱的反应,按下列要求进行了实验的设计与分析:
【实验目的】证明酸和碱发生了中和反应.
【演示实验】将一定量的稀硫酸加入到盛有NaOH溶液的小烧杯中.
【实验原理】该反应的化学方程式为2NaOH+H2SO4=Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,该同学产生了疑问:反应后溶液中的溶质是什么呢?
【实验探究】该同学又选取了BaCl2、酚酞、紫色石蕊溶液设计实验,分别探究上述酸、碱反应后烧杯中溶液中的溶质,取烧杯中溶液,按下列方案进行实验:
①设计的三个方案中,有一个错误的方案是:方案一,该方案错误的原因是即使稀硫酸不过量,也会出现白色沉淀,因为溶液中有生成的硫酸钠,存在硫酸根离子;
②请你简单设计实验对上述错误方案进行更正:取样,滴入几滴紫色石蕊溶液,液变红,溶液呈酸性,说明硫酸过量.
【实验目的】证明酸和碱发生了中和反应.
【演示实验】将一定量的稀硫酸加入到盛有NaOH溶液的小烧杯中.
【实验原理】该反应的化学方程式为2NaOH+H2SO4=Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,该同学产生了疑问:反应后溶液中的溶质是什么呢?
【实验探究】该同学又选取了BaCl2、酚酞、紫色石蕊溶液设计实验,分别探究上述酸、碱反应后烧杯中溶液中的溶质,取烧杯中溶液,按下列方案进行实验:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 硫酸过量 |
| 方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液颜色为紫色 | 酸碱恰好完全反应 |
| 方案三 | 取样,滴入几滴无色酚酞溶液 | 溶液变红 | 氢氧化钠过量,溶质为氢氧化钠和硫酸钠 |
②请你简单设计实验对上述错误方案进行更正:取样,滴入几滴紫色石蕊溶液,液变红,溶液呈酸性,说明硫酸过量.