题目内容
16.科学是一门以实验为基础的学科,科学所取得的丰硕成果,是与实验的重要作用分不开的.结合下列实验装置图回答问题: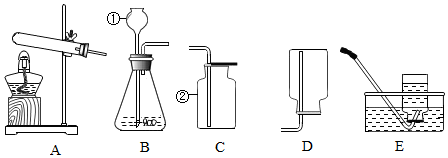
(1)写出指定仪器的名称:②集气瓶
(2)实验室用氯酸钾制取一瓶纯净的氧气时,可选用的发生和收集装置是AC或AE(填字母代号).
(3)在实验过程中,下列操作顺序合理的是②(填序号);
①先加药品、再检查装置的气密性 ②先检查装置的气密性、再加药品
(4)请写出用B装置制取氧气的文字表达式:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
分析 (1)根据实验室常用仪器解答;
(1)根据用氯酸钾和二氧化锰制氧气就需要加热选择发生装置即可;根据氧气的密度比空气大,且不易溶于水进行分析;
(3)根据制取气体的操作步骤进行分析;
(4)根据过氧化氢在二氧化锰做催化剂的条件下生成水和氧气分析解答.
解答 解:(1)根据实验室常用仪器可知:②是集气瓶;
(2)如果用氯酸钾和二氧化锰制氧气就需要加热,故应选用的发生装置是A;氧气的密度比空气大,可用向上排空气法收;氧气不易溶于水,所以可用排水法收集,故收集装置是C或E;
(3)在实验过程中,操作顺序合理的是先检查装置的气密性、再加药品;
(4)用B装置制取氧气时,要用固体二氧化锰和过氧化氢溶液反应,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
故答案为:(1)集气瓶;(2)AC或AE;(3)②;(4)过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写和气体的性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

练习册系列答案
相关题目
7.下列实验操作正确的是(??)
| A. | 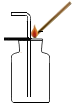 收集二氧化碳并验满 | B. | 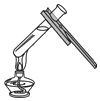 加热液体 | ||
| C. |  取用液体 | D. |  收集氧气 |
11.你认为下列实验方案中,可行的是( )
| A. | 用碱石灰干燥CO2气体 | |
| B. | 向某未知溶液中加入AgNO3溶液,产生白色沉淀,证明溶液是盐酸 | |
| C. | 用稀盐酸浸泡除去久盛石灰水后留下的白色固体 | |
| D. | 将pH试纸润湿后,用玻璃棒蘸取食用白醋滴到试纸上,测定其pH |
1.把干燥的蓝色石蕊试纸放在CO2气体中,石蕊试纸不变色.将CO2气体通入滴有石蕊指示剂的水中,溶液变红色.再将该溶液敞口加热一段时间,发现溶液的红色褪去,冷却到原温度后,再次通人CO2,溶液又变红色.上述实验现象不能说明的是( )
| A. | CO2能和水发生化学反应 | B. | CO2的水溶液具有酸性 | ||
| C. | 加热能使CO2水溶液的酸性减弱 | D. | CO2能使紫色石蕊试液变红 |
5.为了测定某碳酸钠样品(其中杂质为氯化钠)的质量分数,小明同学进行了三次实验,反应的化学方程方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl.实验数据如下表:
根据上表内数据,完成下列有关计算:
(1)碳酸钠样品中碳酸钠的质量是4.24g.
(2)碳酸钠样品中杂质氯化钠的质量分数是15.2%.
(3)加入氯化钙溶液的溶质质量分数是多少?(请根据化学方程式写出完整的计算步骤)
| 编 号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 50 | 50 | 75 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
(1)碳酸钠样品中碳酸钠的质量是4.24g.
(2)碳酸钠样品中杂质氯化钠的质量分数是15.2%.
(3)加入氯化钙溶液的溶质质量分数是多少?(请根据化学方程式写出完整的计算步骤)
3.下列说法中正确的是( )
| A. | 饱和溶液降温析出晶体后,溶质质量分数一定减小 | |
| B. | t℃某饱和的氢氧化钙溶液加入少量的生石灰,充分反应后,恢复到t℃,则溶液的质量不变 | |
| C. | 将密度为1.84 g/cm3溶质质量分数为98%的浓硫酸稀释为49%的硫酸,所加水的体积与所取浓硫酸的体积一定相等 | |
| D. | MgO与CuO的混合物与98g10%的稀硫酸恰好完全反应,则原混合物中氧元素的质量是1.6g |
 ”、“
”、“ ”和
”和 ”分别表示三种不同的分子.试分析回答:
”分别表示三种不同的分子.试分析回答: