题目内容
7.写出下列反应的文字表达式或化学符号表达式(把文字表达式中物质的名称改写为对应的化学式),并回答有关问题.(1)石蜡在空气中燃烧的文字表达式:石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳,常温下呈液态的生成物属于氧化物(填物质类别).
(2)碳酸氢铵固体受热分解的化学符号表达式:NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑,固体应放到试管(填容器名称)中加热.
(3)实验室用双氧水和少量二氧化锰混合物制取氧气的化学符号表达式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,其中二氧化锰的作用是催化作用.
(4)铁在氧气中燃烧的化学符号表达式:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,该反应属于化合反应(填基本反应类型).
分析 石蜡在空气中燃烧生成水和二氧化碳;
碳酸氢铵受热分解生成氨气、水和二氧化碳;
双氧水在二氧化锰的催化作用下分解生成水和氧气;
铁在氧气中燃烧生成四氧化三铁.
解答 解:(1)石蜡在空气中燃烧的文字表达式为:石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳,常温下呈液态的生成物是水,属于氧化物;
(2)碳酸氢铵固体受热分解的化学符号表达式为:NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑,固体应放到试管中加热;
(3)实验室用双氧水和少量二氧化锰混合物制取氧气的化学符号表达式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,其中二氧化锰起到催化作用;
(4)铁在氧气中燃烧的化学符号表达式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,该反应属于化合反应.
故填:石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳;氧化物;NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑;试管;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;催化作用;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;化合.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
18.如图所示的实验操作中,正确的是( )
| A. |  铁在O2中燃烧 | B. |  取粉末于试管 | C. | 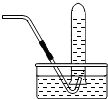 排水法收集氧气 | D. |  干燥氢气 |
2.小明将家中清洗伤口用的消毒液--“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
【第一组实验】检验该双氧水是否失效.
(1)实验过程
①在试管中加入5mL 的“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③如图装置进行操作,带火星的木条复燃,水槽中冰水所起的作用是使氧气中的水蒸气冷凝
(2)实验结论:双氧水没有失效.
【第二组实验】:氧化铜(CuO)能否催化“双氧水”分解
[猜想]Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质不变.
[实验]用天平称量0.2gCuO,取5mL的过氧化氢溶液于试管中,进行如下实验:
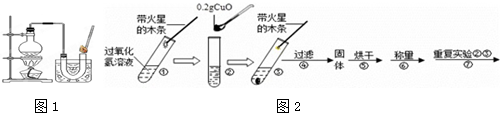
(3)完成下表:
(4)步骤③结束后,用手接触试管底部,感觉烫手.说明“双氧水”分解的化学反应放热(选填“放热”或“吸热”).
(5)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗(带滤纸)、烧杯、玻璃棒.
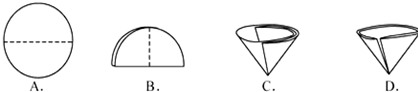
(6)操作④中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是D(填序号).
(7)步骤⑦的目的检验氧化铜化学性质是否改变
(8)过氧化氢能被CuO催化分解放出O2的反应表达式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
【第一组实验】检验该双氧水是否失效.
(1)实验过程
①在试管中加入5mL 的“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③如图装置进行操作,带火星的木条复燃,水槽中冰水所起的作用是使氧气中的水蒸气冷凝
(2)实验结论:双氧水没有失效.
【第二组实验】:氧化铜(CuO)能否催化“双氧水”分解
[猜想]Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质不变.
[实验]用天平称量0.2gCuO,取5mL的过氧化氢溶液于试管中,进行如下实验:

(3)完成下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡冒出, 带火星的木条复燃. | 仍为0.2g | 溶液中有气泡放出, 使带火星木条复燃 | 猜想Ⅰ、Ⅱ不成立,猜想Ⅲ成立. |
(5)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗(带滤纸)、烧杯、玻璃棒.
(6)操作④中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是D(填序号).

(7)步骤⑦的目的检验氧化铜化学性质是否改变
(8)过氧化氢能被CuO催化分解放出O2的反应表达式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
12.下列关于摩尔的说法中,正确的是( )
| A. | 摩尔是表示物质质量的单位 | B. | 摩尔是七个基本物理量之一 | ||
| C. | 摩尔是“物质的量”的单位 | D. | 摩尔是微粒的数量单位 |
 如图所示装置的U形管左侧管内固定一支小试管.
如图所示装置的U形管左侧管内固定一支小试管. 小强课后协助实验室老师准备试剂.为了演示教材实验,需要氢氧化钠、氯化钡和硫酸铜溶液.如图所示,小强应该在化学药品柜盐柜中找到氯化钠和硫酸铜溶液柜中找到氯化钡和硫酸铜溶液.
小强课后协助实验室老师准备试剂.为了演示教材实验,需要氢氧化钠、氯化钡和硫酸铜溶液.如图所示,小强应该在化学药品柜盐柜中找到氯化钠和硫酸铜溶液柜中找到氯化钡和硫酸铜溶液.