题目内容
11.实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放就会造成水污染.于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如下: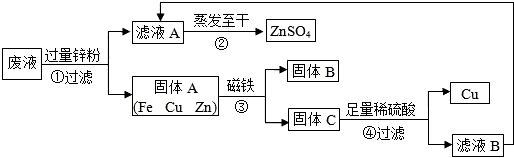
请回答:
(1)滤液A和滤液B含有相同的溶质,其名称是硫酸锌.
(2)写出步骤①其中一个反应的化学方程式Zn+FeSO4═ZnSO4+Fe,或Zn+CuSO4═ZnSO4+Cu;步骤④发生反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑.
分析 锌比铁活泼,铁比铜活泼;
锌能和硫酸亚铁反应生成硫酸锌和铁,能和硫酸铜反应生成硫酸锌和铜,能和稀硫酸反应生成硫酸锌和氢气.
解答 解:(1)锌和硫酸亚铁反应生成硫酸锌和铁,和硫酸铜反应生成硫酸锌和铜,锌和稀硫酸反应生成硫酸锌和氢气,因此滤液A和滤液B含有相同的溶质,其名称是硫酸锌.
故填:硫酸锌.
(2)锌和硫酸亚铁反应生成硫酸锌和铁,和硫酸铜反应生成硫酸锌和铜,锌和稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为:Zn+FeSO4═ZnSO4+Fe,Zn+CuSO4═ZnSO4+Cu,Zn+H2SO4═ZnSO4+H2↑.
故填:Zn+FeSO4═ZnSO4+Fe,或Zn+CuSO4═ZnSO4+Cu;Zn+H2SO4═ZnSO4+H2↑.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
1.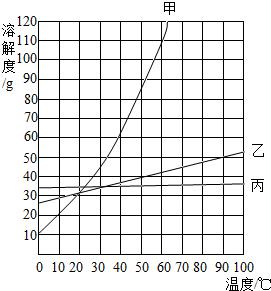 根据下列溶解度表和溶解度曲线图回答问题:
根据下列溶解度表和溶解度曲线图回答问题:
(1)图中硝酸钾的溶解度曲线是甲.
(2)50℃时,乙的溶解度为40g.
(3)60℃时,将甲、乙、丙的固体各20g分别加入50g水中充分溶解后,能形成饱和溶液的是丙.
(4)影响KNO3溶解度的因素是A.
A.温度 B.压强 C.水的质量.
 根据下列溶解度表和溶解度曲线图回答问题:
根据下列溶解度表和溶解度曲线图回答问题:| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| KNO3溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(2)50℃时,乙的溶解度为40g.
(3)60℃时,将甲、乙、丙的固体各20g分别加入50g水中充分溶解后,能形成饱和溶液的是丙.
(4)影响KNO3溶解度的因素是A.
A.温度 B.压强 C.水的质量.
19.有关碳单质及其氧化物的说法中错误的是( )
| A. | 金刚石、石墨、C60互称为碳的同素异形体 | |
| B. | 空气中混有一氧化碳气体,遇明火可能会爆炸 | |
| C. | 碳具有可燃性,只要温度达到着火点即可燃烧 | |
| D. | 用碳素墨水绘制的古代墨画能流传至今不褪色,是因为常温下碳的化学性质稳定 |
16.下列变化中,不属于化学变化的是( )
| A. | 高炉炼铁 | B. | 粮食酿酒 | C. | 灯泡发光 | D. | 燃放礼花 |
3.逻辑推理是化学学习中常用的一种思维方式,以下推理正确的是( )
| A. | 酸雨的pH小于7,所以pH小于7的雨水一定是酸雨 | |
| B. | 氢气与空气混合遇明火可能发生爆炸,所以点燃可燃性气体之前一定要验纯 | |
| C. | 化合物是由不同种元素组成的物质,所以由不同种元素组成的物质一定是化合物 | |
| D. | 化学变化前后物质的总质量不变,所以物质的总质量不变的变化一定是化学变化 |
1.只有当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生.仿照示例填表:
| 反应物(Ⅰ) | 反应物(Ⅱ) | 发生复分解反应的化学方程式(各举一例) | |
| 示例 | 酸 | 碱 | HCl+NaOH═NaCl+H2O |
| A | 盐 | 酸 | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
| B | 碱 | 盐 | Na2CO3+Ca(OH)2=2NaOH+CaCO3↓ |
| C | 氧化物 | 酸 | Fe2O3+6HCl=2FeCl3+3H2O |
| D | 盐 | 盐 | CuSO4+BaCl2═BaSO4↓+CuCl2 |