题目内容
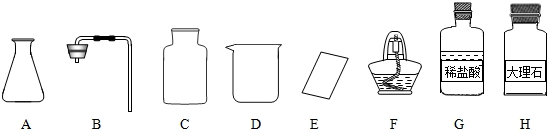
 某同学利用如图装置进行如下实验(装置气密性良好).
某同学利用如图装置进行如下实验(装置气密性良好).(1)若关闭K2,打开K1,将用凸透镜聚光加热锥形瓶中的白磷,充分反应后冷却到室温,观察到的现象是
(2)若关闭K2,打开K1,将气球中的固体加入到锥形瓶的液体中,观察到气球先变瘪,一段时间后恢复原状,则固体和液体可能是
(3)若将气球中9g白色固体加入到锥形瓶中,与足量稀硫酸充分反应生成二氧化碳4.4g.则9g白色固体的组成可能是
①Na2CO3 ②NaHCO3和NaCl
③Na2CO3和NaCl ④Na2CO3和NaHCO3.
考点:反应现象和本质的联系,氧气的化学性质,溶解时的吸热或放热现象,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:实验性简答题
分析:(1)锥形瓶中白磷燃烧放出热量,使瓶内气体急剧膨胀,所以气球先膨胀,燃烧熄灭后,冷却到室温,由于白磷熄消耗瓶内氧气,瓶内气体减少,压强减小,所以气球有变小;写出反应的化学方程式;
(2)根据硝酸铵固体溶于水吸热,使瓶内气体压强减小,所以气球变小解答;
(3)根据生成4.4g二氧化碳所需的白色固体质量解答.
(2)根据硝酸铵固体溶于水吸热,使瓶内气体压强减小,所以气球变小解答;
(3)根据生成4.4g二氧化碳所需的白色固体质量解答.
解答:解:
(1)锥形瓶中白磷燃烧放出热量,使瓶内气体急剧膨胀,所以气球先膨胀,燃烧熄灭后,冷却到室温,由于白磷燃烧消耗瓶内氧气,瓶内气体减少,压强减小,所以气球有变小;反应的化学方程式4P+5O2
2P2O5
(2)硝酸铵固体溶于水吸热,使瓶内气体压强减小,所以气球有变小,一段时间后恢复原状;
(3)设生成4.4g二氧化碳所需的碳酸钠为x
Na2CO3~CO2
106 44
x 4.4g
=
x=10.6g
设生成4.4g二氧化碳所需的碳酸氢钠为y
NaHCO3~CO2
84 44
y 4,4g
=
y=8.4g
故选②④
答案:
(1)白磷燃烧产生大量白烟,气球先变鼓后变瘪 4P+5O2
2P2O5
(2)硝酸铵和水
(3)②④
(1)锥形瓶中白磷燃烧放出热量,使瓶内气体急剧膨胀,所以气球先膨胀,燃烧熄灭后,冷却到室温,由于白磷燃烧消耗瓶内氧气,瓶内气体减少,压强减小,所以气球有变小;反应的化学方程式4P+5O2
| ||
(2)硝酸铵固体溶于水吸热,使瓶内气体压强减小,所以气球有变小,一段时间后恢复原状;
(3)设生成4.4g二氧化碳所需的碳酸钠为x
Na2CO3~CO2
106 44
x 4.4g
| 106 |
| x |
| 44 |
| 4.4g |
x=10.6g
设生成4.4g二氧化碳所需的碳酸氢钠为y
NaHCO3~CO2
84 44
y 4,4g
| 84 |
| y |
| 44 |
| 4.4g |
y=8.4g
故选②④
答案:
(1)白磷燃烧产生大量白烟,气球先变鼓后变瘪 4P+5O2
| ||
(2)硝酸铵和水
(3)②④
点评:本题考查了燃烧的条件,对空气中氧气的测定以及质量守恒定律,让学生通过实验探究去理解、掌握这些知识.

练习册系列答案
相关题目
“低碳生活”是指返璞归真地去进行人与自然的活动,要求减少生活作息时间所消耗的能量,从而减低碳的排放.下列活动不符合“低碳生活”的是( )
| A、使用一次性筷子,减少疾病传染 |
| B、教科书循环使用 |
| C、短时间不使用电脑,将其转为休眠模式 |
| D、用传统发条式闹钟代替电子钟 |

 如图是A、B、C三种固体物质的溶解度曲线.
如图是A、B、C三种固体物质的溶解度曲线. 热水瓶用久后,瓶胆内壁常附着一层水垢(主要成份是CaCO3和Mg(OH)2,其它成份忽略不计).某兴趣小组的同学为了探究水垢中Mg(OH)2的含量,取10g水垢样品,向样品中加入足量的稀盐酸,其变化关系如图所示,试计算:
热水瓶用久后,瓶胆内壁常附着一层水垢(主要成份是CaCO3和Mg(OH)2,其它成份忽略不计).某兴趣小组的同学为了探究水垢中Mg(OH)2的含量,取10g水垢样品,向样品中加入足量的稀盐酸,其变化关系如图所示,试计算: Na2CO3与盐酸反应分两步进行:
Na2CO3与盐酸反应分两步进行: