题目内容
有一瓶已混入碳酸钠的氯化钠固体。学习小组的
 同学为
同学为 了测定该固体中氯化钠的质量分数,取
了测定该固体中氯化钠的质量分数,取
一定量的固体样品于质量为48.82g的烧杯中,
然后逐步加入稀盐酸。当加入25g稀盐酸时反
应恰好完成,加入稀盐酸的质量与烧杯及烧杯
内的物质的总质量关系如右图所示。
(1)该实验取用的样品质量为 g;
(2)该样品中氯化钠的质量分数。
(1)10(1分)
(2)根据质量守恒定律,反应后生成CO2气体的质量为:
58.82g+25g-83.6g=0.22g (1分)
设样品中含Na2CO3的质量为X
2HCl + Na2CO3 = 2NaCl + 2H2O+CO2↑ (1分,不标↑不扣分)
106 44
X 0.22g
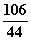 =
=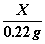 (
( 1分)
1分)
X=0.53g (1分)
样品中含氯化钠的质量为:10g-0.53g=9.47g
样品中氯化钠的质量分数为: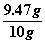 ×100%=94.7%
×100%=94.7%  (1分)
(1分)

练习册系列答案
相关题目
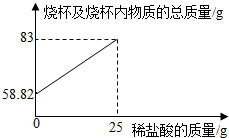 (2013?梧州模拟)有一瓶已混入碳酸钠的氯化钠固体.学习小组的同学为了测定该固体中氯化钠的质量分数,取一定量的固体样品于质量为48.82g的烧杯中,然后逐步加入稀盐酸.当加入25g稀盐酸时反应恰好完成,加入稀盐酸的质量与烧杯及烧杯内的物质的总质量关系如图所示.
(2013?梧州模拟)有一瓶已混入碳酸钠的氯化钠固体.学习小组的同学为了测定该固体中氯化钠的质量分数,取一定量的固体样品于质量为48.82g的烧杯中,然后逐步加入稀盐酸.当加入25g稀盐酸时反应恰好完成,加入稀盐酸的质量与烧杯及烧杯内的物质的总质量关系如图所示.