题目内容
20.如图是某实验中各物质间的转化关系,请据图回答下列问题:
(1)写出氧化铜与稀硫酸反应的化学方程式H2SO4+CuO═CuSO4+H2O.
(2)气体C的化学式是H2,制取气体C的化学方程式Fe+H2SO4═FeSO4+H2↑.属于置换反应(填基本反应类型).
(3)溶液D中一定含有的溶质是FeSO4(写化学式).
分析 (1)氧化铜与稀硫酸反应生成硫酸铜和水,写出反应的化学方程式即可.
(2)氧化铜与硫酸反应生成硫酸铜和水,一氧化碳与氧化铜反应生成铜和二氧化碳,溶液A为硫酸铜与硫酸的混合溶液,B为铁和铜的混合物,铁与稀硫酸反应生成硫酸亚铁和氢气,进行分析解答.
(3)铁与稀硫酸反应生成硫酸亚铁和氢气,铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜,得到固体纯净物E,E应为铜,进行分析解答.
解答 解:(1)氧化铜与稀硫酸反应生成硫酸铜和水,反应的化学方程式为:H2SO4+CuO═CuSO4+H2O.
(2)氧化铜与硫酸反应生成硫酸铜和水,一氧化碳与氧化铜反应生成铜和二氧化碳,溶液A为硫酸铜与硫酸的混合溶液,B为铁和铜的混合物,铁与稀硫酸反应生成硫酸亚铁和氢气,气体C为氢气,其化学式是H2;反应的化学方程式为Fe+H2SO4═FeSO4+H2↑,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
(3)铁与稀硫酸反应生成硫酸亚铁和氢气,铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜,得到固体纯净物E,E应为铜,则溶液D中一定含有的溶质是硫酸亚铁,其化学式为:FeSO4.
故答案为:(1)H2SO4+CuO═CuSO4+H2O;(2)H2;Fe+H2SO4═FeSO4+H2↑;置换反应;(3)FeSO4.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.有一包白色固体可能含有碳酸钙、硫酸铵、碳酸钠、氢氧化钡,将此固体粉末放入足量水中溶解,除有刺激性气味的气体产生外,出现的白色沉淀只有部分可溶于稀硝酸.则原白色固体内( )
| A. | 一定含有硫酸铵、碳酸钠、氢氧化钡 | |
| B. | 一定不含有碳酸钙、碳酸钠、氢氧化钡 | |
| C. | 可能同时含有碳酸钙和碳酸钠 | |
| D. | 可能含有硫酸铵和氢氧化钡 |
11.下列反应属于复分解反应的是( )
| A. | Fe+CuSO4═FeSO4+Cu | B. | CO2+2NaOH═Na2CO3+H2O | ||
| C. | Na2CO3+Ca(OH)2═CaCO3↓+2NaOH | D. | H2CO3═H2O+CO2↑ |
8.下列实验设计合理的是A
| 选项 | 实验目的 | 实验设计 |
| A | 鉴别氢氧化钠和水 | 取样后,分别滴加酚酞溶液后振荡 |
| B | 鉴别生石灰和碳酸钙粉末 | 观察颜色 |
| C | 鉴别空气和氧气 | 闻气体气味 |
| D | 鉴别木炭和铁粉 | 用磁铁吸引 |
12.下列各组中的物质混合,形成溶液的质量比反应前溶液的总质量减少的是( )
| A. | 铜和硝酸银溶液 | B. | 氢氧化铜和稀硫酸 | ||
| C. | 氢氧化钠和稀盐酸 | D. | 氢氧化钾和硝酸钠 |
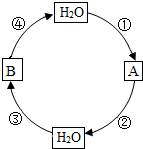 化学兴趣小组设计出以水为主题的“化学反应接龙”游戏.游戏的规则为:用前一个反应的一种生成物作为下一个反应的反应物,并按序号和要求的基本反应类型循环(如图所示).
化学兴趣小组设计出以水为主题的“化学反应接龙”游戏.游戏的规则为:用前一个反应的一种生成物作为下一个反应的反应物,并按序号和要求的基本反应类型循环(如图所示).