题目内容
11.20℃时,取表中的四种物质各20克,加入到100克水中充分溶解后,有固体剩余的是( )| 常见物质的溶解度(20℃) | ||||
| 物质名称 | 氯酸钾 | 硝酸钾 | 氯化钠 | 蔗糖 |
| 溶解度/克 | 7.4 | 31.6 | 36.0 | 203.9 |
| A. | 氯酸钾 | B. | 硝酸钾 | C. | 氯化钠 | D. | 蔗糖 |
分析 根据20℃时,四种物质的溶解度,由溶解度的含义判断20℃时,20克四种物质加入到100克水中充分溶解的质量,结合饱和溶液与不饱和溶液的转化方法,进行分析解答.
解答 解:在20℃时,取下表中的四种物质各20克,加入到100克水中充分溶解后,氯酸钾的溶解度为7.4g,即该温度下100g水中最多溶解7.4g氯酸钾,则有固体剩余的是氯酸钾.
故答案为:氯酸钾.
点评 本题难度不大,掌握饱和溶液的特征、溶解度的概念、饱和溶液与不饱和溶液的相互转化是正确解答本题的关键.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
1.以下有关溶液的说法:①混合物、②无色、③均一、④化合物、⑤稳定、⑥各部分性质相同,其中正确的是( )
| A. | ①③④⑤ | B. | ②④⑤⑥ | C. | ①②④⑤ | D. | ①③⑤⑥ |
2. 用如图所示的装置制取气体,需满足的条件是( )
用如图所示的装置制取气体,需满足的条件是( )
①反应物是固体;
②反应需要加热;
③制得的气体不易溶于水;
④制取的气体密度比空气大;
⑤制得气体能与空气中氧气反应.
 用如图所示的装置制取气体,需满足的条件是( )
用如图所示的装置制取气体,需满足的条件是( )①反应物是固体;
②反应需要加热;
③制得的气体不易溶于水;
④制取的气体密度比空气大;
⑤制得气体能与空气中氧气反应.
| A. | ①②③④⑤ | B. | ②④⑤ | C. | ①②③ | D. | ①② |
19.下列化学方程式书写正确的是( )
| A. | 2Fe+3H2SO4═Fe2(SO4)3+3H2↑ | B. | H2SO4+Cu(OH)2═CuSO4↓+2H2O | ||
| C. | Cu+2HCl═CuCl2+H2↑ | D. | AgNO3+NaCl═AgCl↓+NaNO3 |
16.原子核内有6个质子和6个中子的一种碳原子的质量为xg,另一种元素R的原子质量为yg.则R的相对原子质量为( )
| A. | yg | B. | $\frac{12x}{y}$g | C. | $\frac{y}{x}$ | D. | $\frac{12y}{x}$ |
3.下列根据实验所得数据绘制的图象中,正确的是( )
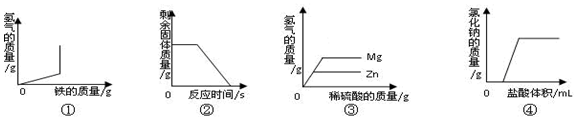

| A. | 图①是将铁粉加入到一定量的稀盐酸中,生成氢气的质量与加入铁粉质量的关系 | |
| B. | 图②是用一定量的木炭还原氧化铜,剩余固体质量与反应时间的关系 | |
| C. | 图③是向等质量的金属镁和锌中加入足量且质量分数相等的稀硫酸,生成氢气的质量与加入稀硫酸质量的关系 | |
| D. | 图④是向久置空气中的NaOH溶液中加入盐酸,生成氯化钠的质量与加入盐酸体积的关系 |
20.下列常见物质中,属于溶液的是( )
| A. | 碘酒 | B. | 泥水 | C. | 植物油 | D. | 牛奶 |
除去下列各物质中混有的少量杂质,所用试剂和操作均正确的是
序号 | 物质 | 杂质 | 所用试剂和操作方法 |
A | CaCO3 | CaO | 高温充分煅烧 |
B | H2 | HCl | 依次通过足量的NaOH溶液、浓硫酸 |
C | NaCl固体 | 细沙 | 加足量的水溶解、过滤 |
D | 铁粉 | Fe2O3 | 加入适量的稀盐酸,过滤、洗涤、干燥 |
A. A B. B C. C D. D