题目内容
现有部分元素的原子结构特点如表:
| X | L层电子数是K层电子数的3倍 |
| Y | 核外电子层数等于原子序数 |
| Z | L层电子数是K层和M层电子数之和 |
| W | 共用三对电子形成双原子分子,常温下为气体单质 |
(1)画出W原子结构示意图________________________________________________。
(2)元素X与元素Z相比,非金属性较强的是__________,写出一个能表示X、Z非金属性强弱关系的化学反应方程式
__________________________________________________________ ______________。
______________。
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为__________。
(4)元素X和元素Y以原子个数比1∶1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式________________________________________________________________________。
答案 (1)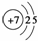
(2)X(或氧) 2H2S+O2 2H2O+2S↓
2H2O+2S↓
(3)NH4HSO4
(4)N2H4+2H2O2 N2↑+4H2O
N2↑+4H2O
解析 L层电子数是K层电子数的3倍,即L层有6个电子,故X为氧元素;核外电子层数等于原子序数的元素只有氢,故Y为氢元素;Z元素的K、L层分别有2个和8个电子,则M层上有6个电子,故Z为硫元素;常温下为气态双原子分子,且原子间以叁键结合的只有N2,故W为氮元素。问题(2)中能说明氧比硫非金属性强的事实有很多,其中较为直观的是O2置换H2S中的S。问题(4)中H、O形成的原子个数比为1∶1的化合物是H2O2,N、H形成的化合物分子中电子数也为18的分子只能是N2H4。

 三种金属能发生下列反应:X + H2SO4 == XSO4 + H2↑
三种金属能发生下列反应:X + H2SO4 == XSO4 + H2↑  Co放射源首次实现了国内批量生产。另外,钴还有多种原子,如
Co放射源首次实现了国内批量生产。另外,钴还有多种原子,如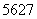 Co、
Co、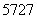 Co、
Co、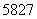 Co和
Co和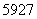 Co。下列关于钴原子的说法正确的是 ( )
Co。下列关于钴原子的说法正确的是 ( )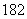 O与D
O与D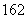 O的相对分子质量相同
O的相对分子质量相同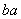 Xn-,下列说法正确的是 ( )
Xn-,下列说法正确的是 ( )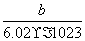 g
g