题目内容
20.向CuSO4溶液中加入过量的锌片,充分反应后,可看到的现象是锌片的表面出现红色物质,溶液由蓝色变为无色,如图表示该反应前后溶液中存在的主要离子,图形“ ”代表的离子是SO42-(填离子符号).
”代表的离子是SO42-(填离子符号).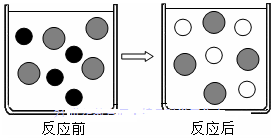
分析 锌与硫酸铜溶液反应生成硫酸锌溶液和铜,微观上锌与铜离子反应生成锌离子和铜,进行分析解答.
解答 解:向CuSO4溶液中加入过量的锌片,锌与硫酸铜溶液反应生成硫酸锌溶液和铜,可看到的现象是锌片的表面出现红色物质,溶液由蓝色变为无色;微观上锌与铜离子反应生成锌离子和铜,图形“ ”反应前后不变,则表示的是硫酸根离子,其离子符号为:SO42-.
”反应前后不变,则表示的是硫酸根离子,其离子符号为:SO42-.
故答案为:锌片的表面出现红色物质,溶液由蓝色变为无色;SO42-.
点评 本题难度不大,掌握金属的化学性质、反应的微观实质是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.栀子花开,淡淡的清香.香满校园的原因是( )
| A. | 分子是由原子构成的 | B. | 分子的质量和体积都很小 | ||
| C. | 分子在不停的运动 | D. | 分子之间有间隔 |
8.稀释浓硫酸时,正确操作是( )
| A. | 将水缓缓倒入盛有浓硫酸的烧杯中,边倒边搅拌 | |
| B. | 将浓硫酸缓缓倒入盛有水的量筒中,边倒边搅拌 | |
| C. | 将浓硫酸缓缓和水一起倒入烧杯中,边倒边搅拌 | |
| D. | 将浓硫酸缓缓倒入盛有水的烧杯中,边倒边搅拌 |
5.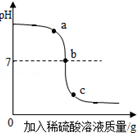 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )
 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )| A. | 图中c点所示溶液呈碱性 | |
| B. | 图中a点所示溶液中,含有的溶质是Na2SO4和H2SO4 | |
| C. | 该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中 | |
| D. | 由a点到b点的pH变化过程证明酸和碱发生了反应 |
12.以下科学实验中,操作正确的是( )
| A. |  | B. |  | C. | 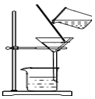 | D. | 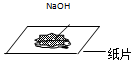 |
10.有一包白色固体,可能含有Na2CO3一种白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中滴加盐酸,沉淀完全溶解并有气体产生.由此推断白色固体中( )
| A. | 可能存在NaOH | B. | 可能存在Na2SO4 | ||
| C. | 肯定不存在BaCl2 | D. | 肯定存在Na2CO3和Na2SO4 |