题目内容
3. A~F均为初中化学常见的物质,已知:A、C是组成元素完全相同的化合物,C通常为液体,D为无色气体,F是白色难溶固体,其中金属元素的质量分数为40%.它们之间有如图所示的转化关系(部分物质和反应条件已略去).
A~F均为初中化学常见的物质,已知:A、C是组成元素完全相同的化合物,C通常为液体,D为无色气体,F是白色难溶固体,其中金属元素的质量分数为40%.它们之间有如图所示的转化关系(部分物质和反应条件已略去).(1)A为过氧化氢(或H2O2),
(2)E物质在生活中的一种用途是改良酸性土壤(或做建筑材料等,答案合理即可);
(3)反应②的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
分析 根据A、C是组成元素完全相同的化合物,C通常为液体,A可以反应生成B和C,因此A为过氧化氢,C为水,B是氧气;氧气反应产生的D是气体,D和F反应产生的F,F是一种难溶性的白色固体,其中金属元素的质量分数为40%,因此F是碳酸钙,则D是二氧化碳,E是氢氧化钙,反应①为水和氧化钙的反应产生氢氧化钙,至此各物质鉴定完毕,带入验证符合题意,可以据此解答.
解答 解:A、C是组成元素完全相同的化合物,C通常为液体,A可以反应生成B和C,因此A为过氧化氢,C为水,B是氧气;氧气反应产生的D是气体,D和F反应产生的F,F是一种难溶性的白色固体,其中金属元素的质量分数为40%,因此F是碳酸钙,则D是二氧化碳,E是氢氧化钙,反应①为水和氧化钙的反应产生氢氧化钙,至此各物质鉴定完毕,带入验证符合题意,因此:
(l)A为过氧化氢溶液;故填:过氧化氢(或H2O2);
(2)E是氢氧化钙,可以改良酸性土壤或做建筑材料等;故填:改良酸性土壤(或做建筑材料等,答案合理即可);
(3)反应②是二氧化碳和氢氧化钙反应产生碳酸钙沉淀和水;故反应的方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
点评 此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论.

练习册系列答案
相关题目
13.长期吸食或注射毒品会危害人体健康甚至危及生命,下列物质都属于毒品的是( )
| A. | 海洛因、黄连素 | B. | 冰毒、大麻 | C. | 甲醛、鸦片 | D. | 摇头丸、黄曲霉素 |
18.下列关于水的变化中,与其他变化有根本区别的一种是( )
| A. | 蒸发水 | B. | 电解水 | C. | 冰雪融化 | D. | 水结成冰 |
12.二氧化碳与二氧化硫同为非金属氧化物,某兴趣小组用类比法进行如下探究:
探究一 SO2的制取
(1)实验室常用固体亚硫酸钠(Na2SO3)与稀硫酸在常温下反应制取二氧化硫,选择发生装置主要应该考虑的因素是A、B(填序号,可多选).
A.反应物的状态 B.反应条件 C.气体密度 D.气体溶解性
(2)探究二氧化硫性质,该兴趣小组进行了如图1所示的实验.
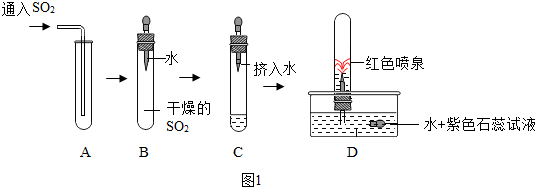
通过上述实验,可推测SO2气体的性质有:
①SO2密度比空气大.
②SO2能溶于水等合理答案.
探究二 CO2和SO2性质的比较
兴趣小组设计并进行如图2实验,探究比较CO2和SO2的化学性质.
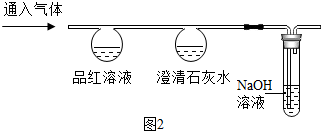
(3)由实验可知:
①二氧化硫能与澄清石灰水反应,生成亚硫酸钙(CaSO3)和水,写出该反应的化学方程式SO2+Ca(OH)2=CaSO3↓+H2O.
②鉴别CO2和SO2的方法是将气体分别通入品红溶液,红色褪去是SO2,无明显变化的是CO2③实验Ⅱ中NaOH溶液的作用是吸收尾气,防止其吸收尾气,防止其污染空气.
探究三 测定空气中SO2的含量,探究小组进行如下实验
【查阅资料】①碘水遇淀粉变蓝色.
②二氧化硫与碘水反应的化学方程式为:SO2+I2+2H2O=H2SO4+2HI
(SO2、I2的相对分子质量分别为:64、254).
③我国环境空气质量标准中对每次空气质量测定中SO2最高浓度限值
(4)测定步骤:
Ⅰ.检查装置的气密性.
Ⅱ.向试管中加入1g溶质质量分数为0.0127%的碘水,用适量的蒸馏水稀释,再滴入2-3滴淀粉溶液,配制成稀溶液.
Ⅲ.在指定地点用注射器抽取空气140次注入上述试管中(假设每次抽气500mL)
由实验可知:
①当溶液由蓝色变成无色时反应恰好完全.
②由此可计算空气中SO2的含量0.46mg/m3(结果精确至0.01),所测地点的空气中SO2的含量属于二级标准(填上表中所列举的等级).
探究一 SO2的制取
(1)实验室常用固体亚硫酸钠(Na2SO3)与稀硫酸在常温下反应制取二氧化硫,选择发生装置主要应该考虑的因素是A、B(填序号,可多选).
A.反应物的状态 B.反应条件 C.气体密度 D.气体溶解性
(2)探究二氧化硫性质,该兴趣小组进行了如图1所示的实验.

通过上述实验,可推测SO2气体的性质有:
①SO2密度比空气大.
②SO2能溶于水等合理答案.
探究二 CO2和SO2性质的比较
兴趣小组设计并进行如图2实验,探究比较CO2和SO2的化学性质.

| 实验Ⅰ | 实验Ⅱ | |
| 通入CO2 | 通入SO2 | |
| 品红溶液 | 无明显变化 | 红色褪为无色 |
| 澄清石灰水 | 白色浑浊 | 白色浑浊 |
①二氧化硫能与澄清石灰水反应,生成亚硫酸钙(CaSO3)和水,写出该反应的化学方程式SO2+Ca(OH)2=CaSO3↓+H2O.
②鉴别CO2和SO2的方法是将气体分别通入品红溶液,红色褪去是SO2,无明显变化的是CO2③实验Ⅱ中NaOH溶液的作用是吸收尾气,防止其吸收尾气,防止其污染空气.
探究三 测定空气中SO2的含量,探究小组进行如下实验
【查阅资料】①碘水遇淀粉变蓝色.
②二氧化硫与碘水反应的化学方程式为:SO2+I2+2H2O=H2SO4+2HI
(SO2、I2的相对分子质量分别为:64、254).
③我国环境空气质量标准中对每次空气质量测定中SO2最高浓度限值
| SO2最高浓度限值(单位mg/m3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
Ⅰ.检查装置的气密性.
Ⅱ.向试管中加入1g溶质质量分数为0.0127%的碘水,用适量的蒸馏水稀释,再滴入2-3滴淀粉溶液,配制成稀溶液.
Ⅲ.在指定地点用注射器抽取空气140次注入上述试管中(假设每次抽气500mL)
由实验可知:
①当溶液由蓝色变成无色时反应恰好完全.
②由此可计算空气中SO2的含量0.46mg/m3(结果精确至0.01),所测地点的空气中SO2的含量属于二级标准(填上表中所列举的等级).
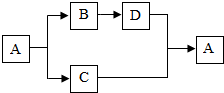 A、B、C、D都是初中化学中常见的物质,具有如图所示的转化关系(反应条件、反应物及生成均已略去).
A、B、C、D都是初中化学中常见的物质,具有如图所示的转化关系(反应条件、反应物及生成均已略去).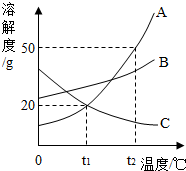 如图为A、B、C三种固体物质的溶解度曲线,请回答
如图为A、B、C三种固体物质的溶解度曲线,请回答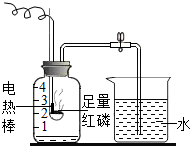 如图所示的是初中化学中的一个重要实验.请回答下列问题:
如图所示的是初中化学中的一个重要实验.请回答下列问题: