题目内容
18.某化学反应用A+B═C+D表示,试回答下列问题:(1)假设反应前有12克A和8克B,反应后生成10克C,A完全消耗,B剩余2克,则生成D8克;
(2)参加化学反应的各物质的质量总和为18克,反应后生成的各物质的质量总和为18克,这个反应符合质量守恒定律;
(3)欲使B完全反应,必须再加入A4克.
分析 根据质量守恒定律,参加反应的各物质的质量之和等于生成的各物质的质量之和,结合题意,进行分析解答.
解答 解:(1)假设反应前有12克A和8克B,反应后生成10克C,A完全消耗,B剩余2克,则生成D的质量为12g+(8g-2g)-10g=8g.
(2)参加化学反应的各物质的质量总和为12g+(8g-2g)=18g;反应后生成的各物质的质量总和为18g,这个反应符合质量守恒定律.
(3)根据题意,参加反应的A和B的质量比为12g:(8g-2g)=2:1;欲使B完全反应,设必须再加入A的质量为x,$\frac{2}{1}$=$\frac{x}{2g}$ x=4g.
故答案为:(1)8;(2)18;18;质量守恒;(3)4.
点评 本题难度不大,掌握质量守恒定律并能灵活运用是正确解答本题的关键.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
13.实验操作有误或不规范,很可能造成失败甚至酿成事故.下列实验操作正确的是( )
| A. | 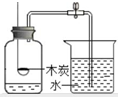 测量氧气含量 | B. | 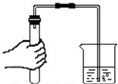 检验装置气密性 | C. |  验满氧气 | D. | 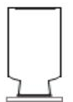 存放氧气 |
3.饮料中的果味大多来自酯类.丁酸乙酯(C6H12O2)是无色具有菠萝香味的液体,常用作食品、饮料的调香剂.有关叙述中正确的是( )
| A. | 丁酸乙酯是由20个原子构成的 | |
| B. | 丁酸乙酯的相对分子质量为116 g | |
| C. | 丁酸乙酯中碳元素的质量分数为62.1% | |
| D. | 一个丁酸乙酯分子中,碳、氢、氧原子的个数比为18:3:8 |
10.某变质的氢氧化钙中含有碳酸钙杂质,称取研细的样品12.4g放入锥形瓶中,加入32.6g的水.充分振荡形成悬浊液,再向锥形瓶中逐滴滴加稀盐酸使其充分反应至无气泡产生,测得加入盐酸的质量与锥形瓶中的物质的质量关系如下表:
请计算:
(1)产生二氧化碳的质量是2.2g;
(2)求样品中氢氧化钙的质量分数(精确到0.1%).
| 加入稀盐酸的质量/g | 0 | 20 | 42.7 |
| 锥形瓶中物质的质量/g | 45 | 65 | 84.4 |
(1)产生二氧化碳的质量是2.2g;
(2)求样品中氢氧化钙的质量分数(精确到0.1%).
7.下列物质中属于纯净物的是( )
| A. | 汽车尾气 | B. | 液态空气 | C. | 清澈的河水 | D. | 水蒸气 |
8. 水和溶液在生命活动和生产、生活中起着十分重要的作用.
水和溶液在生命活动和生产、生活中起着十分重要的作用.
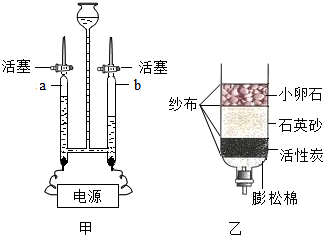
(1)电解水的实验掲示了水的组成.其反应的符号表达式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;甲图中检验a玻璃管内产生气体的方法是将带火星的木条伸入试管中,复燃则证明是氧气.
(2)某同学自制如图乙所示简易净水器,图中活性炭的主要作用是吸附.
(3)衣服上沾有的油污可用汽油洗去,是因为汽油能溶解(填“溶解”或“乳化”)油污.
(4)根据如表回答问题:
①20℃时,向两个分别盛有35g硝酸钾和氯化铵的烧杯中,各加入lOOg水,充分溶解后,为饱和溶液的是硝酸钾溶液;
②只用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液.下列说法正确的是BD.
A.溶液中溶质的质量不变 B.溶液中溶质的质量分数可能增大
C.溶液的质量可能不变 D.可升高温度或增加溶剂.
 水和溶液在生命活动和生产、生活中起着十分重要的作用.
水和溶液在生命活动和生产、生活中起着十分重要的作用.(1)电解水的实验掲示了水的组成.其反应的符号表达式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;甲图中检验a玻璃管内产生气体的方法是将带火星的木条伸入试管中,复燃则证明是氧气.
(2)某同学自制如图乙所示简易净水器,图中活性炭的主要作用是吸附.
(3)衣服上沾有的油污可用汽油洗去,是因为汽油能溶解(填“溶解”或“乳化”)油污.
(4)根据如表回答问题:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 100g水中最多 可溶解/g | 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| 氯化铵 | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
②只用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液.下列说法正确的是BD.
A.溶液中溶质的质量不变 B.溶液中溶质的质量分数可能增大
C.溶液的质量可能不变 D.可升高温度或增加溶剂.