题目内容
15.实验表明浓硫酸与焦炭在加热的条件下能发生反应.经查阅资料得知:①SO2可使澄清石灰水变浑浊;
②SO2可使品红溶液的红色褪去,而CO2不能;
③SO2可与酸性的KMnO4溶液反应使其褪色,而CO2不能;
④CuSO4为白色粉末,遇水可生成胆矾.
⑤浓硫酸与焦炭在加热的条件下发生如下反应:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O
在对该反应的产物的探究中需用下列A、B、C装置:
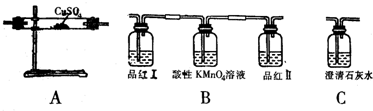
请根据提供的信息回答下列问题:
(1)若要证明这三种产物,正确的组装顺序是ABC,
(2)证明产物CO2的实验现象是品红Ⅱ红色不褪去,C中澄清石灰水变浑浊.
分析 (1)根据按A、B、C的顺序组装分别所起的作用来回答本题;
(2)主要根据二氧化硫与二氧化碳的性质区别来考虑本题.
解答 解:(1)水能使硫酸铜变成蓝色,二氧化硫能使品红褪色,二氧化碳能使澄清的石灰水变浑浊,在检验时先检验水,再检验二氧化硫,然后通过高锰酸钾吸收多余的二氧化硫,再通过品红Ⅱ证明二氧化硫被除尽,最后通过石灰水变浑浊,说明有二氧化碳的存在,因此顺序为ABC;
(2)二氧化硫通过装置B被完全除去后,再将多余的气体通过石灰水变浑浊,石灰水变浑浊,说明有二氧化碳;
故答案为:(1)ABC; (2)品红Ⅱ红色不褪去,C中澄清石灰水变浑浊.
点评 通过回答本题知道了检验水的存在用硫酸铜,能够变蓝即可,检验二氧化硫用品红溶液或高锰酸钾溶液,检验二氧化碳用澄清石灰水.

练习册系列答案
相关题目
3.要使100克10%的食盐水的溶质质量分数增加一倍,可采取的方法是( )
| A. | 再加入10克食盐 | B. | 蒸发掉50克水 | ||
| C. | 蒸发掉45克水 | D. | 再加入100克30%食盐水 |
20.下列有关空气和呼出气体的探究实验的说法中,正确的是( )
| A. | 人吸入的是氧气,呼出的是二氧化碳 | |
| B. | 难以观察到空气使澄清石灰水变浑浊,所以空气中不含二氧化碳 | |
| C. | 观察到燃着的木条在呼出气体中会熄灭,所以呼出气体中不含氧气 | |
| D. | 呼吸过程消耗了氧气,属于缓慢氧化 |
4.混合物分离的方法在生产、生活和科学实验中有着广泛的应用.下列做法中应用了结晶方法的是( )
| A. | 用海水晒盐 | B. | 除去混在铜粉中的铁粉 | ||
| C. | 除去水中的泥沙 | D. | 分离豆浆和豆渣 |
5.下列物质的转化一步反应能实现的是( )
| A. | H2SO4 HCl | B. | SO2 Na2SO4 | C. | Cu(OH)2 NaOH | D. | NaNO3Ba(NO3)2 |
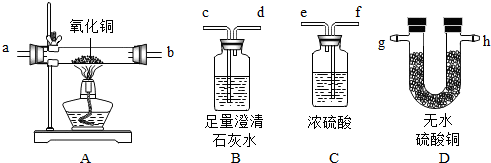
 如图是初中化学实验的几种常用仪器,请按要求填空.
如图是初中化学实验的几种常用仪器,请按要求填空.