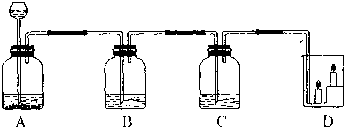题目内容
根据下列描述对D、E成分写出正确的解释
(1)D和E均含两种元素,滴入D产生气泡,反应后E的化学性质、质量不变;D 、E ;
(2)E是白色固体有腐蚀性加入水,在烧杯中同样看到气泡,原因是溶解时 ;
(3)D有腐蚀性PH=0,将D的溶液滴入锥形瓶中,溶液变浅绿色,有气泡产生;烧杯中聚集的肥皂泡能被点燃,锥形瓶中发生反应的化学方程式为 .
(1)D和E均含两种元素,滴入D产生气泡,反应后E的化学性质、质量不变;D
(2)E是白色固体有腐蚀性加入水,在烧杯中同样看到气泡,原因是溶解时
(3)D有腐蚀性PH=0,将D的溶液滴入锥形瓶中,溶液变浅绿色,有气泡产生;烧杯中聚集的肥皂泡能被点燃,锥形瓶中发生反应的化学方程式为
考点:物质的鉴别、推断,催化剂的特点与催化作用,常见碱的特性和用途,书写化学方程式、文字表达式、电离方程式
专题:常见物质的推断题
分析:(1)根据二氧化锰、过氧化强的组成和性质分析回答;
(2)根据氢氧化钠的性质分析回答;
(3)根据硫酸有腐蚀性能与铁反应分析回答.
(2)根据氢氧化钠的性质分析回答;
(3)根据硫酸有腐蚀性能与铁反应分析回答.
解答:解:(1)由于二氧化锰、过氧化强都是由两种元素组成,二氧化锰能使过氧化氢分解放出氧气.所以,由D和E均含两种元素,滴入D产生气泡,反应后E的化学性质、质量不变可知,D是过氧化氢,E是二氧化锰.化学式分别是:H2O2、MnO2;
(2)由于氢氧化钠是白色的固体,有强烈的腐蚀性,在溶于水时能放出大量的热.所以,由E是白色固体有腐蚀性加入水,在烧杯中同样看到气泡可知,E是氢氧化钠,原因是氢氧化钠溶解时放出大量的热;
(3)由于硫酸是一种酸,有腐蚀性,能与铁反应生成了硫酸亚铁和氢气,硫酸亚铁溶液显浅绿色,氢气具有可燃性,密度小.所以,D是硫酸,锥形瓶中发生反应的化学方程式为Fe+H2SO4=FeSO4+H2↑.
故答为:(1)H2O2,MnO2;(2)放出大量的热;(3)Fe+H2SO4=FeSO4+H2↑.
(2)由于氢氧化钠是白色的固体,有强烈的腐蚀性,在溶于水时能放出大量的热.所以,由E是白色固体有腐蚀性加入水,在烧杯中同样看到气泡可知,E是氢氧化钠,原因是氢氧化钠溶解时放出大量的热;
(3)由于硫酸是一种酸,有腐蚀性,能与铁反应生成了硫酸亚铁和氢气,硫酸亚铁溶液显浅绿色,氢气具有可燃性,密度小.所以,D是硫酸,锥形瓶中发生反应的化学方程式为Fe+H2SO4=FeSO4+H2↑.
故答为:(1)H2O2,MnO2;(2)放出大量的热;(3)Fe+H2SO4=FeSO4+H2↑.
点评:本题属于物质的推断题,解决本题的关键是熟悉常见物质的性质、反应的现象等.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
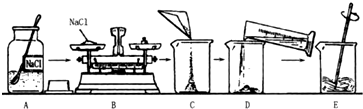
下列实验操作中正确的是( )
A、 滴加试剂 |
B、 液体加热 |
C、 检验CO2是否集满 |
D、 检查装置的气密性 |
中和反应在工农业生产和日常生活中有广泛的用途.下列应用一定与中和反应原理无关的是( )
| A、施用熟石灰改良酸性土壤 |
| B、服用含Al(OH)3的药物治疗胃酸过多 |
| C、用生石灰、硫酸铜和水配制波尔多 |
| D、用NaOH溶液洗涤石油产品中的残余硫酸 |
下列现象和事实,可用金属活动性作出合理解释的是( )
①“真金不怕火炼”;②铝的利用比铜和铁晚;③金属镁和稀盐酸反应比铁剧烈;④波尔多液不宜用铁制容器盛放;⑤常温下,铝比镁更容易与氧气发生化学反应.
①“真金不怕火炼”;②铝的利用比铜和铁晚;③金属镁和稀盐酸反应比铁剧烈;④波尔多液不宜用铁制容器盛放;⑤常温下,铝比镁更容易与氧气发生化学反应.
| A、①③④⑤ | B、②③④⑤ |
| C、①②③④ | D、①②④⑤ |
 (1)“闻香识茶”利用了分子
(1)“闻香识茶”利用了分子