题目内容
15.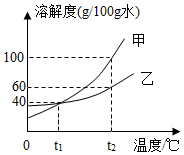 甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示,请回答.
甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示,请回答.①t2℃时,甲、乙两种物质溶解度较大的是甲
②t1℃时,100g水中放入50g乙,充分溶解后所得溶液的质量是140g.
③t2℃时,甲、乙溶液的溶质质量分数相等均为a%,其中一定是不饱和溶液的是甲,a%的取值范围是≤37.5%.
④将t2℃等质量的甲、乙饱和溶液分别降温到t1℃,下列说法正确的是AD.
A.t1℃时溶质质量分数:甲=乙 B.t1℃时溶质质量:甲=乙
C.t1℃时溶剂质量:甲>乙 D.析出晶体质量:甲>乙.
分析 根据溶解度曲线的意义可以,①比较相同温度时(或一定温度范围内)不同物质溶解度的大小,根据饱和溶液的质量分数与溶解度的关系,可判断此时两物质的饱和溶液的溶质质量分数大小;②查出某温度时物质的溶解度,根据溶解度的意义分析判断有关的问题;③比较和确定物质的溶解度受温度影响的程度,利用图示的曲线,判断甲、乙两物质的溶解度随温度降低而改变情况.
解答 解:①由甲、乙两种物质的溶解度曲线可知,t2℃时,甲、乙两种物质溶解度较大的是甲;
②由乙物质的溶解度曲线可知,t1℃时,乙物质的溶解度是40g,t1℃时,100g水中放入50g乙,只能溶解40g,充分溶解后所得溶液的质量是100g+40g=140g.
③由甲、乙两种物质的溶解度曲线可知,t2℃时,甲的溶解度大于乙,乙的溶解度是60g,甲、乙溶液的溶质质量分数相等均为a%,其中一定是不饱和溶液的是甲,a%的取值范围是不大于t2℃时乙的饱和溶液的质量分数,即:$\frac{60g}{100g+60g}×100%$≈37.5%.
④A.由甲、乙两种物质的溶解度曲线可知,甲、乙的溶解度随温度的降低而减小,将t2℃等质量的甲、乙溶液分别降温到t1℃,都是此温度时的饱和溶液,t1℃时甲、乙的溶解度相同,溶质质量分数:甲=乙,故A正确;
B.由上述分析可知,将t2℃等质量的甲、乙溶液分别降温到t1℃,甲的溶解度受温度的影响较大,甲析出固体的质量多,t1℃时溶质质量:甲<乙,故B不正确;
C.将t2℃等质量的甲、乙溶液分别降温到t1℃,甲析出固体的质量多,t1℃时溶剂质量:甲<乙,故C不正确;
D.由上述分析可知,将t2℃等质量的甲、乙溶液分别降温到t1℃,析出晶体质量:甲>乙.故D正确.
故答为:①甲;②140;③甲,≤37.5%;④AD.
点评 本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力.

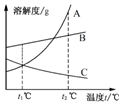
| A. | 可用降温结晶法从A、B、C的固体混合物中提纯A | |
| B. | t2℃时三种饱和溶液降温至t1℃,溶质质量分数:B>A=C | |
| C. | 若A、B、C中有一种是易溶气体溶解度曲线,那一定是C | |
| D. | 用同一种方法能将A、B、C的饱和溶液均变为不饱和溶液 |
| A. | 酒精挥发 | B. | 车胎爆炸 | C. | 干冰升华 | D. | 饭菜变馊 |
| A. | 催化剂就是二氧化锰 | |
| B. | 催化剂能降低物质的化学反应速度 | |
| C. | 在化学反应前后催化剂的状态没有改变 | |
| D. | 催化剂可以使反应物进行反应且反应前后化学性质没有改变 |
| A. | 氧气用于急救病人 | B. | 铁粉用作脱氧剂 | ||
| C. | 干冰用作制冷剂 | D. | 熟石灰用于改良酸性土壤 |
| A. | 二氧化碳通入氢氧化钠溶液中有白色沉淀生成 | |
| B. | 将氧化铜加入稀硫酸中,产生气泡同时溶液变蓝色 | |
| C. | 打开盛有浓盐酸的试剂瓶的瓶盖,瓶口出现白烟 | |
| D. | 氢氧化钠溶液中加入硫酸铜溶液,产生蓝色沉淀 |
 如图中A、B对比说明燃烧需要的条件是燃烧需要氧气(或空气),若B、C同样证明此条件,并且时间短现象明显,可以向烧杯C中最好加入固体、液体为①(填序号)
如图中A、B对比说明燃烧需要的条件是燃烧需要氧气(或空气),若B、C同样证明此条件,并且时间短现象明显,可以向烧杯C中最好加入固体、液体为①(填序号) 某同学在实验室发现一瓶标签残缺的硫酸铜溶液,为了测定此溶液的溶质质量分数,他取出50g该溶液.逐滴加入NaOH溶液,加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题:
某同学在实验室发现一瓶标签残缺的硫酸铜溶液,为了测定此溶液的溶质质量分数,他取出50g该溶液.逐滴加入NaOH溶液,加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题: