题目内容
16.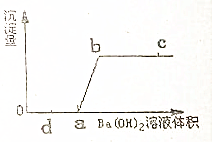 已知某混合液由HCl、Na2CO3、H2SO4、CuCl2溶液中的一种或几种混合而成向该混合液中加Ba(OH)2溶液,产生沉淀与加的Ba(OH)2体积关系如图.请回答:
已知某混合液由HCl、Na2CO3、H2SO4、CuCl2溶液中的一种或几种混合而成向该混合液中加Ba(OH)2溶液,产生沉淀与加的Ba(OH)2体积关系如图.请回答:(1)该混合液中一定含有HCl、CuCl2,一定没有Na2CO3、H2SO4.
(2)oa段发生发应的化学方程式为2HCl+Ba(OH)2=BaCl2+2H2O
ab段发生反应的化学方程式为CuCl2+Ba(OH)2=BaCl2+Cu(OH)2↓
(3)a点对应的溶液中一定含有的溶质为氯化钡、氯化铜
b点对应的溶液中一定含有的溶质为氯化钡
c点对应的溶液中一定含有的溶质为氯化钡、氢氧化钡.
分析 根据产生沉淀量与加的Ba(OH)2溶液体积关系图,开始加入的氢氧化钡并没有出现沉淀,利用硫酸钡既不溶于水又不溶于酸,可判断混合溶液中不含硫酸且一定含有盐酸;根据HCl、Na2CO3、CuCl2、NaCl四种物质中,HCl与Na2CO3不能共存的特点,可判断混合溶液中不含碳酸钠;综合以上情况,可判断实验中所出现的现象为加入的氢氧化钡先与混合溶液中的盐酸反应,待盐酸完成反应后与氯化铜反应生成氢氧化铜沉淀,而氯化钠的存在不影响以上现象的出现,因此混合溶液中可能含有氯化钠.
解答 解:依据产生沉淀量与加的Ba(OH)2溶液体积关系图,开始加入的氢氧化钡并没有出现沉淀,利用硫酸钡既不溶于水又不溶于酸,可判断混合溶液中不含硫酸且一定含有盐酸;根据HCl、Na2CO3、CuCl2、NaCl四种物质中,HCl与Na2CO3不能共存的特点,可判断混合溶液中不含碳酸钠;综合以上情况,可判断实验中所出现的现象为加入的氢氧化钡先与混合溶液中的盐酸反应,待盐酸完成反应后与氯化铜反应生成氢氧化铜沉淀,而氯化钠的存在不影响以上现象的出现,因此混合溶液中可能含有氯化钠,所以
(1)该混合液中一定含有HCl、CuCl2,一定没有Na2CO3、H2SO4;
(2)oa段发生的发应是盐酸和氢氧化钡反应生成氯化钡和水,化学方程式为:2HCl+Ba(OH)2=BaCl2+2H2O;
ab段发生的反应是氯化铜和氢氧化钡反应生成氢氧化铜沉淀和氯化钠,化学方程式为:CuCl2+Ba(OH)2=BaCl2+Cu(OH)2↓;
(3)a点对应的溶液中一定含有的溶质为氯化铜、氯化钡;
b点对应的溶液中一定含有的溶质为氯化钡;
c点对应的溶液中一定含有的溶质为氯化钡、氢氧化钡.
故答案为:(1)HCl、CuCl2,Na2CO3、H2SO4;
(2)2HCl+Ba(OH)2=BaCl2+2H2O;
CuCl2+Ba(OH)2=BaCl2+Cu(OH)2↓;
(3)氯化铜、氯化钡;
氯化钡;
氯化钡、氢氧化钡.
点评 解答本题时要注意:在酸存在情况下,向混合溶液中滴加氢氧化钡既使与氯化铜反应生成了氢氧化铜沉淀,该沉淀也会被酸反应而溶解,因此,所加入氢氧化钡实际上是先消耗混合溶液中的酸.

| A. | 过氧化氢 | B. | 高锰酸钾 | C. | 氯酸钾 | D. | 空气 |
| 编号 | 物质 | 杂质 | 试剂 | 除杂操作方法 |
| A | CO2 | CO | 点燃 | |
| B | NaCl | KNO3 | 水 | 溶解、过滤、蒸发 |
| C | NaNO3 | Na2CO3 | 适量CaCl2溶液 | 过滤 |
| D | Cu | CuO | 过量盐酸 | 过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 用打火机检查液化气罐是否漏气 | |
| B. | 电器设备起火用水扑灭 | |
| C. | 室内起火时马上打开门窗通风 | |
| D. | 厨房煤气管道漏气,迅速关闭阀门并开窗通风 |
| A. | 氢氧化钙用于治疗胃酸过多 | B. | 氧气用作火箭燃料 | ||
| C. | 胆矾用于检验水 | D. | 食盐溶液用于消毒杀菌 |
| 选项 | 物质 | 杂质(少量) | 试剂及操作方法 |
| A | 氧化钙 | 石灰石 | 高温 |
| B | FeCl3溶液 | CuCl2 | 加入过量铁粉、过滤 |
| C | 氯化钠 | 泥沙 | 加入足量的水,溶解、蒸发、结晶 |
| D | H2 | HCl气体 | 先通过足量的NaOH溶液,再通过浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
 溶解度是解决溶液相关问题的重要依据,请根据右图溶解度曲线解决下列问题(M、N均不含结晶水):
溶解度是解决溶液相关问题的重要依据,请根据右图溶解度曲线解决下列问题(M、N均不含结晶水):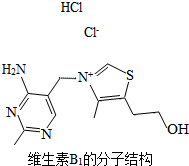 寨卡病毒是一种通过蚊虫进行传播的虫媒病毒,可能出现的典型症状包括低热、斑丘疹、关节疼痛、结膜炎等.用维生素B1泡水擦身可预防蚊虫叮咬,而且没有副作用.维生素B1的化学式为C12H17ClN4OS
寨卡病毒是一种通过蚊虫进行传播的虫媒病毒,可能出现的典型症状包括低热、斑丘疹、关节疼痛、结膜炎等.用维生素B1泡水擦身可预防蚊虫叮咬,而且没有副作用.维生素B1的化学式为C12H17ClN4OS