题目内容
下表是教材中为探究铜、铝和银的金属活动性顺序而设计的实验探究方案,请你填写表中相应的内容:
结论:所探究金属的活动性顺序为: .
| 实验步骤 | 现象 | 反应的化学方程式 |
| 将铝丝浸入硫酸铜溶液中 | ||
| 将铜丝浸入硝酸银溶液中 | ||
| 将铜丝浸入硫酸铝溶液中 | / |
考点:金属活动性顺序及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据将铝丝浸入硫酸铜溶液中、铜丝浸入硝酸银溶液中、铜丝浸入硫酸铝溶液中的反应现象,判断能否发生反应,进而可确定三种金属活动性由强到弱的顺序.
解答:解:将铝丝浸入硫酸铜溶液中,铝丝表面有红色物质析出,溶液变为无色,铝与硫酸铜溶液反应生成硫酸铝溶液和铜,说明铝的金属活动性比铜强,即铝>铜,反应的化学方程式为:2Al+3CuSO4=3Cu+Al2(SO4)3.
将铜丝浸入硝酸银溶液中,铜丝表面有银白色物质析出,溶液变为蓝色,铜与硝酸银溶液反应生成硝酸铜溶液和银,说明铜的金属活动性比银强,即铜>银,反应的化学方程式为:Cu+2AgNO3=2Ag+Cu(NO3)2.
将铜丝浸入硫酸铝溶液中,无明显变化,说明铜的金属活动性比铝弱,即铝>铜.
铝>铜,铜>银,铝>铜,则三种金属的活动性顺序为铝>铜>银.
故答案为:
结论:铝>铜>银.
将铜丝浸入硝酸银溶液中,铜丝表面有银白色物质析出,溶液变为蓝色,铜与硝酸银溶液反应生成硝酸铜溶液和银,说明铜的金属活动性比银强,即铜>银,反应的化学方程式为:Cu+2AgNO3=2Ag+Cu(NO3)2.
将铜丝浸入硫酸铝溶液中,无明显变化,说明铜的金属活动性比铝弱,即铝>铜.
铝>铜,铜>银,铝>铜,则三种金属的活动性顺序为铝>铜>银.
故答案为:
| 实验步骤 | 现象 | 反应的化学方程式 |
| 将铝丝浸入硫酸铜溶液中 | 铝丝表面有红色物质析出,溶液变为无色 | 2Al+3CuSO4=3Cu+Al2(SO4)3 |
| 将铜丝浸入硝酸银溶液中 | 铜丝表面有银白色物质析出,溶液变为蓝色 | Cu+2AgNO3=2Ag+Cu(NO3)2 |
| 将铜丝浸入硫酸铝溶液中 | 无明显现象 | / |
点评:本题难度不大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在含有氯化铜和氯化锌的溶液中加入过量的铁粉,充分反应后过滤,滤纸上的固体物质是( )
| A、Cu |
| B、Cu; Fe |
| C、Fe; Zn |
| D、Cu; Zn |
下列有关催化剂的说法正确的是( )
| A、催化剂加快其他物质反应速率 |
| B、催化剂作为反应物可以参加化学变化 |
| C、催化剂在反应前后质量和化学性质不变 |
| D、二氧化锰是催化剂 |
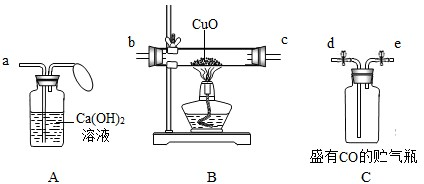 用如图提供的装置和试剂,组装一套用一氧化碳使氧化铜还原成铜的实验装置,并回答问题.
用如图提供的装置和试剂,组装一套用一氧化碳使氧化铜还原成铜的实验装置,并回答问题.