题目内容
13. 如图是实验室电解水的示意图,回答下列问题.
如图是实验室电解水的示意图,回答下列问题.(1)实验中观察到产生的氢气与氧气的体积比为2:1,检验与电源正极相连的试管中产生气体的方法是将带火星的木条伸入产生的气体中,若木条复燃,则生成气体是氧.(写出操作方法、现象与结论)
(2)若电解180克水,计算生成的氢气和氧气的质量分别是多少?生成氢气和氧气的质量比为多少?
分析 根据电解水时,与正极相连的试管生成的气体是氧气,较少.与负极相连的试管生成的是氢气,较多.检验氧气用带火星的木条.根解反应的方程式进行计算.
解答 解:(1)试管中产生的气体较多的是氢气,剩余的是氧气;所以试管中氢气与氧气的气体体积比是2:1;
正极产生的气体是氧气,氧气具有助燃性,能使带火星的木条复燃,检验该气体的方法是将带火星木条伸入试管中,木条复燃;
故答案为:2:1;将带火星的木条伸入产生的气体中,若木条复燃,则生成气体是氧.
(2)设电解180g水生成氢气质量为x,生成氧气质量为y
2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2
36 4 32
180g x y
$\frac{36}{180g}$=$\frac{4}{x}$=$\frac{32}{y}$
x=20g,y=160g
20g:160g=1:8
答:电解180g水可生成20g氢气,160g氧气;生成氢气和氧气的质量之比为1:8.
点评 同学们要熟悉电解水的实验现象和结论,并据此来解决一些常见的问题,此题难度较小.

练习册系列答案
相关题目
1.空气和水是人类宝贵的自然资源,下列关于空气和水的说法正确的是( )
| A. | 明矾可促进水中悬浮杂质的沉降 | |
| B. | 空气中含量最多,且性质稳定的是稀有气体 | |
| C. | 空气的成分按质量分数计算,氧气约占21% | |
| D. | 水的三态(固态、气体、液态)循环过程中没有发生变化的是水分子之间的间隔 |
18.小林在家做“提纯粗盐”的实验,下列分析错误的是( )
| A. | 将粗盐放入水中溶解--粒子在不断运动 | |
| B. | 溶解时用筷子搅拌--加速溶解 | |
| C. | 过滤粗盐水--可将粗盐水变为纯净物 | |
| D. | 实验时不用一次性塑料杯或纸杯--环保低碳,要从小事做起 |
2.1902年诞生于比利时的传统水处理工艺(经典“四部曲”)被美国工程院列为人类20世纪最重要的发明之一,其净水的方法主要有:①过滤,②絮凝,③消毒,④沉淀.下列最为合理的净水顺序是( )
| A. | ②①③④ | B. | ④②①③ | C. | ②④①③ | D. | ②④③① |
3.下列属于化学变化的是( )
| A. | 石蜡融化 | B. | 潮湿的衣服被晾干了 | ||
| C. | 铁生锈 | D. | 瓷碗破碎 |
 根据如图A、B、C三种固体的溶解度曲线回答:
根据如图A、B、C三种固体的溶解度曲线回答: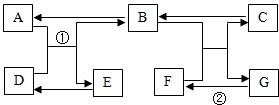 A~G是初中所学的常见物质,其转化关系如下图所示(部分反应物和生成物、反应条件已略去),A、B常温下为无色气体且组成元素相同,C是大理石的主要成分,D为红色固体,E为黑色固体.请回答下列问题:
A~G是初中所学的常见物质,其转化关系如下图所示(部分反应物和生成物、反应条件已略去),A、B常温下为无色气体且组成元素相同,C是大理石的主要成分,D为红色固体,E为黑色固体.请回答下列问题: