题目内容
20.我们生活在一个丰富多彩的物质世界中,人类的生产、生活和化学密不可分.(1)用适当的化学符号填空:
①常用来改良酸性土壤的碱Ca(OH)2 ②汽水中的酸H2CO3
③人体中含量最多的元素O ④硝酸铵中的阳离子NH4+
(2)归纳总结是学习化学的重要方法,小明同学用图1总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).
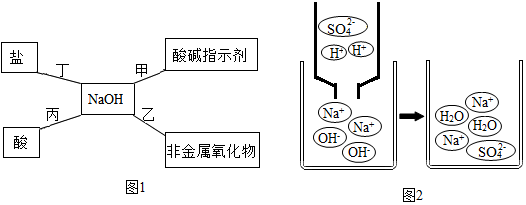
①验证反应甲:小明将无色酚酞溶液滴入NaOH溶液中,溶液呈红色.
②小明用示意图2来说明反应丙的发生,写出该反应的化学方程式:2NaOH+H2SO4═Na2SO4+2H2O.
③请你写出一个化学反应方程式,满足反应丁能够发生CuSO4+2NaOH=Na2SO4+Cu(OH)2↓,该反应的基本类型是复分解反应.
分析 (1)常用来改良酸性土壤的碱是氢氧化钙;汽水中的酸是碳酸;人体中含量最多的元素是氧元素;硝酸铵中的阳离子是铵根离子;
(2)氢氧化钠溶液显碱性,能使酚酞试液变红色;
由示意图2可知,氢氧化钠和稀硫酸反应生成硫酸钠和水;
硫酸铜属于盐,能和氢氧化钠反应生成硫酸钠和氢氧化铜沉淀,属于复分解反应.
解答 解:(1)①常用来改良酸性土壤的碱是氢氧化钙,可以表示为Ca(OH)2;
②汽水中的酸是碳酸,可以表示为H2CO3;
③人体中含量最多的元素是氧元素,可以表示为O;
④硝酸铵中的阳离子是铵根离子,可以表示为NH4+.
故填:Ca(OH)2;H2CO3;O;NH4+.
(2)①验证反应甲:小明将无色酚酞溶液滴入NaOH溶液中,溶液呈红色.
故填:红.
②小明用示意图2来说明反应丙的发生,图中氢氧化钠和稀硫酸反应生成硫酸钠和水,该反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O.
故填:2NaOH+H2SO4═Na2SO4+2H2O.
③硫酸铜属于盐,能和氢氧化钠反应生成硫酸钠和氢氧化铜沉淀,反应的化学方程式为:CuSO4+2NaOH=Na2SO4+Cu(OH)2↓,属于复分解反应.
故填:CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;复分解反应.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
19.下列说法正确的是( )
| A. | 肥皂水能区分食盐水和硬水 | |
| B. | 中和反应生成盐和水,生成盐和水的一定是中和反应 | |
| C. | 化肥中加熟石灰研磨,无刺激性气味,一定不是氮肥 | |
| D. | 饱和溶液析出晶体后,溶质质量减少,溶质的质量分数也一定减小 |
20.下列变化过程中,一定发生了化学变化的是( )
| A. | 用氢氧化钠干燥气体 | B. | 食物腐烂 | ||
| C. | 用活性炭净水器净水 | D. | 用汽油清洗油污 |
9.CO2是造成温室效应增强的主要气体,在工业上可用CO2来制备甲醇等物质.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来并利用,能有效地减少CO2气体的排放.如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出).

下列有关该方法的叙述中正确的是( )

下列有关该方法的叙述中正确的是( )
| A. | 该方法可减少碳排放而且耗能小 | |
| B. | 整个过程中,涉及了四大反应类型 | |
| C. | “反应分离室”中,分离物质的基本操作是蒸发、结晶、过滤 | |
| D. | 该方法的优点是至少有两种物质可以循环利用 |