题目内容
1.写出下列反应的化学方程式:①氯化钡溶液与碳酸钠溶液混合:BaCl2+Na2CO3=BaCO3↓+2NaCl;
②碳酸钠溶液与稀盐酸混合:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
③氢氧化钠溶液与稀硫酸混合:2NaOH+H2SO4═Na2SO4+2H2O.
④盐酸与三氧化二铁Fe2O3+6HCl═2FeCl3+3H2O
⑤铁与稀硫酸Fe+H2SO4═FeSO4+H2↑
⑥石灰水与二氧化碳CO2+Ca(OH)2═CaCO3↓+H2O
⑦石灰水与碳酸钠Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
⑧氨碱法制纯碱原理NH3+CO2+H2O+NaCl═NaHCO3↓+NH4Cl;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
分析 根据反应物、生成物和反应条件及质量守恒定律的两个原则,写出正确的化学方程式.
解答 解:①氯化钡与碳酸钠反应生成碳酸钡和氯化钠,反应的化学方程式为:BaCl2+Na2CO3=BaCO3↓+2NaCl;
②碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑;
③氢氧化钠与稀硫酸反应生成硫酸钠和水,该反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O;
④三氧化二铁与稀盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;
⑤铁与硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑;
⑥二氧化碳与澄清石灰水反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;
⑦氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
⑧氨碱法生产纯碱的化学反应原理是用氨气和二氧化碳与氯化钠饱和溶液反应生成碳酸氢钠,然后加热碳酸氢钠制取碳酸钠;氨气溶于水所得氨水呈碱性,比水更易吸收二氧化碳;在一定温度下,碳酸氢铵的溶解度比氯化铵的溶解度小,故碳酸氢铵能首先从溶液中析出.在受热的条件下,碳酸氢钠分解生成了碳酸钠、水和二氧化碳.发生反应的化学原理是:NH3+CO2+H2O+NaCl═NaHCO3↓+NH4Cl;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
故答案为:①BaCl2+Na2CO3=BaCO3↓+2NaCl;②Na2CO3+2HCl=2NaCl+H2O+CO2↑;③2NaOH+H2SO4═Na2SO4+2H2O;④Fe2O3+6HCl═2FeCl3+3H2O;
⑤Fe+H2SO4═FeSO4+H2↑;⑥CO2+Ca(OH)2═CaCO3↓+H2O;⑦Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;⑧NH3+CO2+H2O+NaCl═NaHCO3↓+NH4Cl;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,掌握化学方程式的书写方法(写、配、注、等)即可正确解答本题.

 阅读快车系列答案
阅读快车系列答案| A. | 磷酸二氢钾是由四种元素组成的 | |
| B. | 磷酸二氢钾中含有八个原子 | |
| C. | 磷酸二氢钾中磷元素的化合价为+5价 | |
| D. | 磷酸二氢钾中氢元素和氧元素的质量比为1:32 |
| A. | 焦炭 | B. | 铁矿石 | C. | 氢气 | D. | 一氧化碳 |
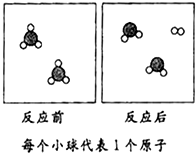
| A. | 该反应是化合反应 | |
| B. | 该反应的反应物一定是氧化物 | |
| C. | 该反应是分解反应 | |
| D. | 该反应中反应物和生成物的分子个数比为1:1:1 |
 根据如图所示甲、乙两种微粒的结构示意图填空.
根据如图所示甲、乙两种微粒的结构示意图填空.

